
Wetenschap
Hoe de massa van reactanten de chemische reactiesnelheid beïnvloedt
Door Diane Evans Bijgewerkt op 30 augustus 2022
De snelheid van een chemische reactie is de snelheid waarmee reactanten in producten worden omgezet. De botsingstheorie legt uit dat reacties voldoende energie vereisen om reactantdeeltjes te laten botsen, bindingen te verbreken en nieuwe verbindingen te vormen. De massa van de reactantdeeltjes beïnvloedt het beschikbare oppervlak voor botsingen en beïnvloedt daarmee de reactiesnelheid.
Reactiepercentages
Verschillende factoren, zoals massa, concentratie, temperatuur en deeltjesgrootte, bepalen hoe snel een reactie verloopt. Kleinere, lichtere deeltjes bieden meer oppervlak voor botsingen, waardoor de snelheid toeneemt. Daarentegen kunnen grote, complexe moleculen met afgelegen reactieve locaties langzaam reageren, zelfs als botsingen frequent voorkomen.
Concentratie
Het verhogen van de concentratie van reactanten versnelt doorgaans een reactie omdat er in de loop van de tijd meer deeltjes beschikbaar zijn om met elkaar te botsen. Voor reacties waarbij grote biomoleculen zoals eiwitten betrokken zijn, vertalen hogere concentraties zich echter niet altijd in snellere snelheden, omdat de reactieve plaatsen verborgen kunnen zijn in de moleculaire structuur.
Temperatuur
Warmte levert kinetische energie, waardoor de deeltjessnelheid en de botsingsfrequentie toenemen. Kleine, lichtgewicht deeltjes hebben minder warmte nodig om de energiedrempel te bereiken, terwijl overmatige hitte grote eiwitten kan denatureren, waardoor hun structuur wordt verstoord en de reactiviteit wordt verminderd.
Deeltjesgrootte en massa
Wanneer een vaste reactant fijngemalen wordt tot een poeder, neemt het oppervlak ervan toe, waardoor meer reactieve plaatsen bloot komen te liggen en de reactiesnelheid toeneemt. Grafisch gezien begint de reactievoortgang vaak snel wanneer de concentraties hoog zijn en neemt deze geleidelijk af naarmate de reactanten worden verbruikt, om uiteindelijk te stagneren wanneer de reactie voltooid is.
Hoofdlijnen
- Wat is de Disc-diffusiemethode die wordt gebruikt bij antibacteriële activiteit?
- Unieke pigmenten in de fotosynthetische mariene bacterie onthullen hoe hij leeft bij weinig licht
- Een genetische eigenschap die aanwezig is maar ongezien in een persoon die een eigenschap wordt genoemd?
- Een bacteriën die van vorm kunnen veranderen, worden opgeroepen?
- Nieuw onderzoek laat zien hoe wetenschappers sociale media gebruiken
- Wat de relatie tussen DNA en chromosomen?
- Wat is de genetische definitie van evolutie?
- Biotische delen van een ecosysteem interageren met?
- Wat zijn enkele manieren waarop mensen de balansfotosynthese en cellulaire ademhaling verstoren?
- Voedingswetenschappers maken gezonde probiotische drank van sojapulp

- Katalysatoronderzoek voor zonnebrandstoffen:amorf molybdeensulfide werkt het beste

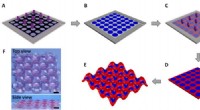
- Hydrogels met periodiek patroon:een model voor coöperatieve vervorming
- Vergroening van biomaterialen en steigers die worden gebruikt in regeneratieve geneeskunde

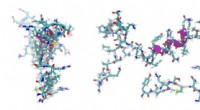
- Mechanochemische vorming van peptidebindingen achter de oorsprong van het leven
 Waarom gaat energie verloren tussen voedingsniveaus?
Waarom gaat energie verloren tussen voedingsniveaus?  Onderzoekers ontwikkelen model voor het voorspellen van aardverschuivingen veroorzaakt door aardbevingen
Onderzoekers ontwikkelen model voor het voorspellen van aardverschuivingen veroorzaakt door aardbevingen Hoeveel lichtjaren per jaar?
Hoeveel lichtjaren per jaar?  Gevonden:een nauwkeurige methode om te bepalen hoe golven en deeltjes fusiereacties beïnvloeden
Gevonden:een nauwkeurige methode om te bepalen hoe golven en deeltjes fusiereacties beïnvloeden Hoe klimaatverandering bijdraagt aan wereldwijd geweld
Hoe klimaatverandering bijdraagt aan wereldwijd geweld Welke fysieke hoeveelheid komt overeen met de snelheid van stroomlaad?
Welke fysieke hoeveelheid komt overeen met de snelheid van stroomlaad?  Hoe kunt u onderscheid maken tussen zwaveldioxide en chloor met behulp van blauw lakmuspapier?
Hoe kunt u onderscheid maken tussen zwaveldioxide en chloor met behulp van blauw lakmuspapier?  Afbeelding:Frosty krater op Mars
Afbeelding:Frosty krater op Mars
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com


