
Wetenschap
Wat is een chemische buffer?
Hier is hoe het werkt:
* buffersysteem: Een buffersysteem bestaat uit een zwak zuur en de conjugaatbasis, of een zwakke basis en het geconjugeerde zuur.
* evenwicht: Het zwakke zuur/base en het geconjugeerde paar bestaan in een evenwicht. Wanneer een zuur wordt toegevoegd, reageert de basis in het buffersysteem met de toegevoegde H+ -ionen om meer van het zwakke zuur te vormen, waardoor de verandering in pH wordt geminimaliseerd. Evenzo, wanneer een basis wordt toegevoegd, reageert het zuur in het buffersysteem met de toegevoegde oh-ionen om meer van de conjugaatbasis te vormen, waardoor de verandering in pH opnieuw wordt geminimaliseerd.
* Buffercapaciteit: Een buffer heeft een beperkte capaciteit om pH -veranderingen te weerstaan. De hoeveelheid zuur of base die het kan neutraliseren voordat de pH aanzienlijk verandert, wordt de buffercapaciteit genoemd. Dit hangt af van de concentratie van de buffercomponenten.
Voorbeelden van chemische buffers:
* bicarbonaatbuffer: Dit systeem is cruciaal bij het handhaven van de bloed -pH bij mensen. Het bestaat uit carbonzuur (H2CO3) en bicarbonaationen (HCO3-).
* fosfaatbuffer: Dit buffersysteem is belangrijk bij intracellulaire vloeistoffen. Het bestaat uit dihydrogen fosfaat (H2PO4-) en waterstoffosfaat (HPO42-) ionen.
Belang van chemische buffers:
* Biologische systemen: Buffers zijn essentieel voor het handhaven van de pH van biologische vloeistoffen, zoals bloed, cytoplasma en urine. Dit is cruciaal voor de juiste werking van enzymen en andere biologische processen.
* Chemische reacties: Buffers worden vaak gebruikt in chemische reacties om een specifieke pH te behouden, wat belangrijk kan zijn voor de reactiesnelheid en opbrengst.
* Industriële toepassingen: Buffers worden gebruikt in verschillende industriële toepassingen, zoals bij voedselproductie, cosmetica en farmaceutische producten.
Sleutelconcepten gerelateerd aan chemische buffers:
* pH: Een maat voor de zuurgraad of alkaliteit van een oplossing.
* PKA: De dissociatieconstante van een zwak zuur, dat de sterkte ervan aangeeft.
* Henderson-Hasselbalch-vergelijking: Deze vergelijking relateert de pH van een bufferoplossing voor de PKA van het zwakke zuur en de verhouding van de concentraties van het zuur en de conjugaatbasis ervan.
Door te begrijpen hoe buffers werken, kunnen we hun belang waarderen in verschillende contexten, van biologische systemen tot industriële processen.
 Lading van P als een ion?
Lading van P als een ion?  Welke stoffen zijn moeilijk te classificeren als vaste stoffen of vloeistoffen?
Welke stoffen zijn moeilijk te classificeren als vaste stoffen of vloeistoffen?  Hoe nanobubbels van gas de reacties tussen vaste stoffen en vloeistoffen versnellen
Hoe nanobubbels van gas de reacties tussen vaste stoffen en vloeistoffen versnellen  Wetenschappers maken 3D-geprinte, microscopisch kleine gassensoren:schilderspallets zonder een vleugje pigment
Wetenschappers maken 3D-geprinte, microscopisch kleine gassensoren:schilderspallets zonder een vleugje pigment Innovatieve technieken voor DNA-herstel kunnen slachtoffers helpen verkrachters in Kenia te pakken
Innovatieve technieken voor DNA-herstel kunnen slachtoffers helpen verkrachters in Kenia te pakken
 De uitstoot van broeikasgassen in Brazilië daalt met 2,3 procent in 2017
De uitstoot van broeikasgassen in Brazilië daalt met 2,3 procent in 2017 Oude muizentanden laten zien dat nederzettingen al lang vóór de landbouw een ecologische impact hadden
Oude muizentanden laten zien dat nederzettingen al lang vóór de landbouw een ecologische impact hadden  Taiwan getroffen door talloze aardbevingen, waarvan de sterkste een kracht van 6,3 bereikte
Taiwan getroffen door talloze aardbevingen, waarvan de sterkste een kracht van 6,3 bereikte  Wetenschappers:wind, droogte verergert branden, geen slecht management
Wetenschappers:wind, droogte verergert branden, geen slecht management NASA vindt tropische storm Bebinca boven Laos, Thailand
NASA vindt tropische storm Bebinca boven Laos, Thailand
Hoofdlijnen
- Wat is het verschil tussen rode bloedcellen en witte cellen?
- Welk fenotype wordt geproduceerd door AA -genotype?
- Welk organisme veroorzaakte de Ierse Patato -plaag?
- Is het menselijk weefsel een geleider of geleiding?
- Wat hindert sprinkhanen?
- Factoren die de groei van micro-organismen beïnvloeden
- Welke polymeren coderen voor een kenmerk van een organisme?
- Een AI-model om de onzekerheid in de voorspelling van de verdamping te verminderen
- Wat is de groep organismen die voedsel maken voor een ecosysteem?
- Nieuw polymeer kan de prestaties van organische en perovskiet-zonnecellen verbeteren

- Gepulseerde elektronenbundels werpen licht op de productie van kunststoffen

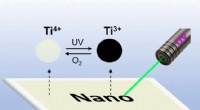
- Schrijven met licht op titanium:herschrijfbare UV-gevoelige oppervlakken gemaakt van gedoteerde TiO2-nanokristallen
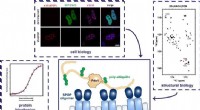
- Hoe weet een regulerend eiwit waar het moet binden om de insulineproductie te moduleren?
- Oog knipperend op een chip

 Wat is chemische carbonatatie?
Wat is chemische carbonatatie?  Wat zijn de overeenkomsten tussen vogels en zoogdieren?
Wat zijn de overeenkomsten tussen vogels en zoogdieren?  Uit gegevens van MAXI J1820+070 blijkt dat Einstein gelijk had over hoe materie in een zwart gat stort
Uit gegevens van MAXI J1820+070 blijkt dat Einstein gelijk had over hoe materie in een zwart gat stort  Wat heeft de volgende generatie telescoop nodig om leven te detecteren?
Wat heeft de volgende generatie telescoop nodig om leven te detecteren?  In Athene, zeldzame sneeuwdekens Akropolis, stopt vaccinaties
In Athene, zeldzame sneeuwdekens Akropolis, stopt vaccinaties Hoe specifieke geleidbaarheid naar zoutgehalte om te zetten
Hoe specifieke geleidbaarheid naar zoutgehalte om te zetten Wat is de enige taxonomische categorie die bestaat als een discrete eenheid in de natuur?
Wat is de enige taxonomische categorie die bestaat als een discrete eenheid in de natuur?  Welke eigenschappen kunnen worden waargenomen tijdens een chemische reactie?
Welke eigenschappen kunnen worden waargenomen tijdens een chemische reactie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

