
Wetenschap
Kopersulfaat en water:het hydratatieproces begrijpen
1. Ontbinding:
- Kopersulfaat, een ionische verbinding, lost op in water. De watermoleculen omringen de koper(II)-ionen (Cu²⁺) en sulfaationen (SO₄²⁻) en verbreken de ionische bindingen die ze bij elkaar houden.
2. Hydratatie:
- De watermoleculen vormen vervolgens gecoördineerde covalente bindingen met de koper(II)-ionen. Dit betekent dat het zuurstofatoom van het watermolecuul een paar elektronen afstaat aan het koperion.
- Deze bindingen zijn sterker dan de oorspronkelijke ionische bindingen in het vaste kopersulfaat.
3. Vorming van Aqua Complex:
- De gehydrateerde koper(II)-ionen vormen een complex ion genaamd het hexaaquakoper(II)-ion ([Cu(H₂O)₆]²⁺). Het koper(II)-ion is omgeven door zes watermoleculen.
- De sulfaationen worden ook gehydrateerd, maar hun interactie met water is minder dramatisch.
Algehele reactie:
CuSO₄(s) + 6 H₂O(l) → [Cu(H₂O)₆]²⁺(aq) + SO₄²⁻(aq)
Gevolgen:
- Kleurverandering: Kopersulfaatkristallen zijn wit of lichtblauw. Wanneer ze oplossen en hydrateren, krijgt de oplossing een helderblauwe kleur. Dit komt door de absorptie van bepaalde golflengten van licht door het hexaaquakoper(II)-ion.
- Warmteverandering: Het hydratatieproces is exotherm, wat betekent dat er warmte vrijkomt.
- Geleidbaarheid: De oplossing wordt elektrisch geleidend vanwege de aanwezigheid van de vrije ionen.
Belangrijke opmerking:
- Kopersulfaat kan in verschillende gehydrateerde vormen voorkomen. De meest voorkomende is koper(II)sulfaatpentahydraat (CuSO₄·5H₂O), dat vijf watermoleculen per kopersulfaatmolecuul bevat.
Laat het me weten als je nog vragen hebt!
 Wat is het effect van langzaam neutronen op nucleaire reacties?
Wat is het effect van langzaam neutronen op nucleaire reacties?  Als P-32 bèta-verval ondergaat, betekent dit dat atomen wat worden?
Als P-32 bèta-verval ondergaat, betekent dit dat atomen wat worden?  Waarom gedragen leden van een gezinselementen hetzelfde in chemische reacties?
Waarom gedragen leden van een gezinselementen hetzelfde in chemische reacties?  De elektronen in de binding tussen waterstof en fluor worden sterker aangetrokken tot welk atoom?
De elektronen in de binding tussen waterstof en fluor worden sterker aangetrokken tot welk atoom?  Kopersulfaat en water:het hydratatieproces begrijpen
Kopersulfaat en water:het hydratatieproces begrijpen
 Wat is een klein bos?
Wat is een klein bos?  Tropische storm let op in Guam, NASA ziet 02W-vorm
Tropische storm let op in Guam, NASA ziet 02W-vorm Als we een man op de maan kunnen zetten, we kunnen het Great Barrier Reef redden
Als we een man op de maan kunnen zetten, we kunnen het Great Barrier Reef redden Maken levende wezens en niet -levende een ecosysteem op?
Maken levende wezens en niet -levende een ecosysteem op?  Tropische cycloon of ISU-cycloon? Semantische wetenschappelijke zoekmachine weet dat er een verschil is
Tropische cycloon of ISU-cycloon? Semantische wetenschappelijke zoekmachine weet dat er een verschil is
Hoofdlijnen
- Wanneer ziektekiemen het lichaam binnengaan, wat zijn antilichamen geproduceerd door?
- Waarom gebruikten wetenschappers Drosophila voor chromosomale studies?
- Hoeveel genen zijn er in DNA?
- Wat zou er met een voedselketen gebeuren als er ziekte zou zijn?
- Wat doet een bioloog op typische dag?
- Wat is een voorbeeld van Oomycota?
- Lijst van forensische technieken
- Waar verwijst de term Bacillus naar?
- Wat hebben de processen van fotosynthese en celademhaling gemeen?
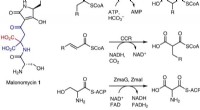
- Wetenschappers ontdekken nieuwe route naar antibiotica met behulp van genbewerking
- Kristaloorlogen:onderzoek kan leiden tot efficiëntere methoden voor kristaltechnologie

- Wetenschappers maken een atomair lijmpistool om betere nucleïnezuurtherapieën te bouwen
- Zeemosselen zijn een model voor het verbeteren van kracht, rekbaarheid en hechting in hydrogels voor wondgenezing

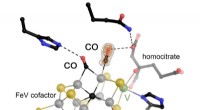
- Vanadiumafhankelijke stikstofase kan twee CO-moleculen tegelijk binden
 Zijn milieuwetenschappers zich geen zorgen over methoden om natuurlijke hulpbronnen te behouden?
Zijn milieuwetenschappers zich geen zorgen over methoden om natuurlijke hulpbronnen te behouden?  Wanneer voorspellingen van theoretische chemici werkelijkheid worden
Wanneer voorspellingen van theoretische chemici werkelijkheid worden Hoe beïnvloedt het klimaat het type bioom dat in een gebied helpt?
Hoe beïnvloedt het klimaat het type bioom dat in een gebied helpt?  Zuidwest VS bruist terwijl experts record Thanksgiving voorspellen
Zuidwest VS bruist terwijl experts record Thanksgiving voorspellen Waarom heeft het universum zichzelf niet vernietigd? Neutrino's kunnen het antwoord bevatten
Waarom heeft het universum zichzelf niet vernietigd? Neutrino's kunnen het antwoord bevatten Hoeveel werk wordt er gedaan als 12N Force 0,5 m beweegt?
Hoeveel werk wordt er gedaan als 12N Force 0,5 m beweegt?  Wie is de slimste ster?
Wie is de slimste ster?  Waarom gas heeft geen duidelijk volume?
Waarom gas heeft geen duidelijk volume?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

