
Wetenschap
Inzicht in pH en ijzer:waarom ijzer geen pH heeft
* pH is een maatstaf voor de zuurgraad of alkaliteit van een oplossing. Het wordt gedefinieerd als de negatieve logaritme van de waterstofionenconcentratie ([H+]) in een oplossing.
* IJzer is een metaal. Het is een vast element en bestaat niet in een oplossing waarin waterstofionen kunnen worden gemeten.
Je kunt het echter wel hebben over de pH van oplossingen die ijzerverbindingen bevatten:
* IJzerzouten: Wanneer ijzer reageert met zuren, vormt het zouten zoals ijzerchloride (FeCl3) of ijzersulfaat (FeSO4). Deze zouten kunnen, wanneer opgelost in water, de pH van de oplossing beïnvloeden. De pH zal afhangen van het specifieke zout en de concentratie ervan.
* IJzeroxiden: IJzeroxiden zijn, net als roest (Fe2O3), onoplosbaar in water, maar kunnen reageren met zuren. Deze reacties kunnen de pH van de oplossing beïnvloeden.
Daarom is het niet zinvol om over de pH van ijzer zelf te praten. U moet de specifieke ijzerverbinding en de vorm ervan in oplossing specificeren om de pH te bepalen.
 Wat is het verschil tussen een bergketen en systeem?
Wat is het verschil tussen een bergketen en systeem?  Feiten over de Oceanische Zone
Feiten over de Oceanische Zone  NASA kijkt naar tropische storm Son-Tinh die het eiland Hainan treft, China
NASA kijkt naar tropische storm Son-Tinh die het eiland Hainan treft, China Technologie kan bodemherstel na olielozingen helpen versnellen
Technologie kan bodemherstel na olielozingen helpen versnellen Nachtelijke satellietbeelden van NASA-NOAA onthullen de ontwikkeling van tropische storm Josephine
Nachtelijke satellietbeelden van NASA-NOAA onthullen de ontwikkeling van tropische storm Josephine
Hoofdlijnen
- Bloedgroep en uw hartgezondheid:belangrijkste bevindingen uit recente onderzoeken
- E. coli Actief transport:kalium- en hypertone oplossingen
- Hoe kan een hormoon dat in zeer kleine hoeveelheden in de bloedbaan aanwezig is, zo'n grote responscel opwekken?
- Wat zijn enkele problemen waarmee mensen zouden worden geconfronteerd als er geen bacteriën waren?
- Wat is de cellulaire structuur van een protist?
- Wat is de wetenschappelijke theorie achter de celtheorie?
- DNA-replicatiecontrole begrijpen:oorsprong en initiatoreiwitten
- Welk type stamcel kan aanleiding geven tot een in het lichaam?
- Hoe verschillen schimmelsporen van bacteriële endosporen?
- Een gemakkelijke weg naar polymeercoatings met potentieel gebruik bij het voorkomen van biofouling
- Milieu-impact van antivries:effecten op dieren in het wild, planten en bodem

- Zwak gebonden zout is een belangrijk ingrediënt voor zeer zuivere Li@C60-film

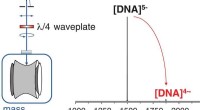
- Massaspectrometrie gebruiken om guaninerijke DNA-ionen te isoleren
- Bierafval scheiden in eiwitten voor voedingsmiddelen, en vezels voor biobrandstoffen

 Wat is het bereik van luchtdruk?
Wat is het bereik van luchtdruk?  Hoe werkt een seismograaf? Wat is de schaal van Richter?
Hoe werkt een seismograaf? Wat is de schaal van Richter?  Algoritme kan helpen de populariteit van posts op sociale media te vergroten
Algoritme kan helpen de populariteit van posts op sociale media te vergroten Onderzoekers onderzoeken erosie en veerkracht van rivieroevers aan de kust van Bangladesh
Onderzoekers onderzoeken erosie en veerkracht van rivieroevers aan de kust van Bangladesh Fabricage van fotonische kristallen op nanoschaal met een ultrasnelle laser
Fabricage van fotonische kristallen op nanoschaal met een ultrasnelle laser  Hoe beïnvloeden de huidige milieuproblemen het gebruik van hernieuwbare energie?
Hoe beïnvloeden de huidige milieuproblemen het gebruik van hernieuwbare energie?  Hoe zonnebrillen werken
Hoe zonnebrillen werken  Tekstboekformules voor het beschrijven van warmtestroomkarakteristieken, cruciaal in veel industrieën, zijn te eenvoudig, studie toont
Tekstboekformules voor het beschrijven van warmtestroomkarakteristieken, cruciaal in veel industrieën, zijn te eenvoudig, studie toont
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

