
Wetenschap
Netto-ionvergelijkingen onder de knie krijgen:een stapsgewijze handleiding
Door Luc Braybury – Bijgewerkt op 30 augustus 2022
Een netto-ionische vergelijking vangt alleen de ionen op die daadwerkelijk deelnemen aan een chemische reactie, waarbij de onveranderde “toeschouwer”-ionen worden weggelaten. Het is het meest bruikbaar voor reacties die plaatsvinden in een waterige oplossing, waarbij sterke elektrolyten volledig dissociëren in ionen en elektriciteit geleiden, terwijl zwakke elektrolyten of niet-elektrolyten minimaal bijdragen aan het ionengehalte.
Stap 1 – Schrijf de volledig uitgebalanceerde vergelijking
Begin met de volledige reactie. Bijvoorbeeld:
CaCl2 (aq) + 2AgNO3 (aq) → Ca(NO3 )2 (aq) + 2AgCl(s)
Stap 2 – Converteren naar de totale ionenvergelijking
Geef elke sterke elektrolyt weer als de samenstellende ionen. Zwakke elektrolyten blijven als hele moleculen achter.
Ca 2+ + 2Cl – + 2Ag + + 2NO3 – → Ca 2+ + 2NO3 – + 2AgCl(s)
Stap 3 – Verwijder de toeschouwerionen om de netto-ionenvergelijking te verkrijgen
Identificeer ionen die aan beide kanten van de vergelijking onveranderd lijken. Hier, Ca 2+ en NEE3 – zijn toeschouwers.
2Cl – (aq) + 2Ag + (aq) → 2AgCl(s)
 Twee miljoen jaar oud ijs geeft een momentopname van de geschiedenis van broeikasgassen op aarde
Twee miljoen jaar oud ijs geeft een momentopname van de geschiedenis van broeikasgassen op aarde NASA vindt orkaan Lees krachtverschuiving
NASA vindt orkaan Lees krachtverschuiving Nieuwe studie verklaart de koudste temperaturen van Antarctica
Nieuwe studie verklaart de koudste temperaturen van Antarctica De natuur moet centraal staan in de economie, zeggen onderzoekers
De natuur moet centraal staan in de economie, zeggen onderzoekers IJs op het Antarctisch Schiereiland stabieler dan gedacht
IJs op het Antarctisch Schiereiland stabieler dan gedacht
Hoofdlijnen
- Wat betekent de uitdrukkingsdichtheid van receptorcellen?
- Wat zijn de 10 biologische takken van de wetenschap?
- Wat is de definitie die ten grondslag ligt aan ziekte?
- Welke soorten klinische monsters kunnen een gemengde flora opleveren in bacteriële culturen?
- Celdeling die vervolgens volgt, biedt nieuwe cellen zodat wat kan gebeuren?
- Wat doet de plant met producten van fotosynthese?
- Komt de evolutie op het niveau van organismen op?
- Zou de ontdekking van een sleutelgensysteem de laatste zucht van koralen kunnen verstikken?
- Wat zijn zeer wetenschappelijke woorden?
- Onderzoekers maken de weg vrij voor het maken van een nieuw type MRI-contrastmiddel

- Tomaten van dezelfde kwaliteit als normaal, maar met slechts de helft van het water

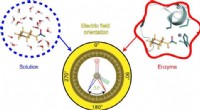
- Elektrische velden in kaart brengen om te helpen ontrafelen hoe enzymen werken
- Organische kristallen ijsvormende superkrachten

- Therapeutische geluidsgolven krijgen door dikke schedels

 Wat is elektronenconfiguratie van een atoom?
Wat is elektronenconfiguratie van een atoom?  Wat bacteriën ons kunnen leren over het bestrijden van atrazinebesmettingen
Wat bacteriën ons kunnen leren over het bestrijden van atrazinebesmettingen  Wetenschappers proberen oude slachtmethoden na te bootsen en leren hoe Neanderthalers vogels aten
Wetenschappers proberen oude slachtmethoden na te bootsen en leren hoe Neanderthalers vogels aten  Video:Het historische avontuur van Cassini-Huygens
Video:Het historische avontuur van Cassini-Huygens Wat is min 10 graden Celsius gelijk aan in Fahrenheit?
Wat is min 10 graden Celsius gelijk aan in Fahrenheit?  Telegram beschuldigt Apple van het blokkeren van updates
Telegram beschuldigt Apple van het blokkeren van updates Hoge uitstoot van broeikasgassen uit Siberische binnenwateren
Hoge uitstoot van broeikasgassen uit Siberische binnenwateren Wat is een atoombinding?
Wat is een atoombinding?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

