
Wetenschap
De wetenschap achter de waterstofbinding van water
Door Diane EvansBijgewerkt op 30 augustus 2022
Water bevat twee verschillende soorten bindingen:covalente bindingen die de zuurstof- en waterstofatomen binnen elk molecuul bij elkaar houden, en waterstofbruggen die het ene watermolecuul met het andere verbinden. De covalente bindingen geven water zijn moleculaire structuur, terwijl de waterstofbruggen het netwerk creëren dat de bulkeigenschappen van de vloeistof definieert.
Waterstofbinding in vloeibaar water
In vloeibaar water zijn waterstofbruggen relatief zwak, maar hun enorme aantal domineert het gedrag van het molecuul. Ze ontstaan door elektrostatische aantrekking tussen de gedeeltelijk positieve waterstofatomen en de gedeeltelijk negatieve zuurstofatomen. Omdat de moleculen voortdurend in beweging zijn, worden deze bindingen dynamisch gevormd en verbroken. Verwarming verhoogt de moleculaire kinetische energie, waardoor de neiging van bindingen om te breken wordt versterkt en water kan verdampen. In de gasfase drijven watermoleculen onafhankelijk; zodra ze zijn afgekoeld, herstellen de waterstofbruggen zich en wordt de vloeistof opnieuw gevormd.
Waterstofbinding in ijs
IJs neemt een kristallijn rooster aan waarin elk watermolecuul tetraëdrisch wordt gecoördineerd door vier buren via waterstofbruggen. Deze geordende opstelling beperkt de moleculaire beweging, waardoor ijs minder dicht is dan vloeibaar water. Als gevolg hiervan drijft het ijs en vormt het een beschermende deken over watermassa's die het waterleven in de winter ondersteunt.
Water als oplosmiddel
De polariteit van water – een ongelijkmatige verdeling van de lading veroorzaakt door het elektronegatieve zuurstofatoom – zorgt ervoor dat het ionen en polaire moleculen kan omringen en scheiden. Door de kleine omvang van watermoleculen kunnen veel ervan zich rond een opgeloste stof clusteren, waardoor waterstofbruggen worden gevormd die de opgeloste stof uit elkaar trekken. Dit verklaart waarom water meer stoffen oplost dan welke andere vloeistof dan ook, en daarmee de titel ‘universeel oplosmiddel’ verdient.
Fysische eigenschappen van water
Waterstofbinding zorgt voor een hoge cohesie en oppervlaktespanning, wat duidelijk wordt wanneer druppels op met was behandelde oppervlakken parelen. Het is ook verantwoordelijk voor de hoge verdampingswarmte van water, waardoor zweten een effectief koelmechanisme voor zoogdieren is. De grote energie die nodig is om waterstofbruggen te verbreken, betekent dat water over een breed temperatuurbereik vloeibaar blijft, wat de levensprocessen ondersteunt.
Waterstofbinding in biologische systemen
Naast zelfinteractie bindt water waterstofbruggen met moleculen die hydroxyl- (OH) of amine- (NH₂)-groepen bezitten, een kenmerk dat cruciaal is voor talloze biochemische reacties. Het vermogen van water om structuren te stabiliseren en moleculen te transporteren, in combinatie met zijn thermische buffercapaciteit, is onmisbaar geweest voor de evolutie van het leven op aarde.
 Wat is het verschil smeltpunt van natriumjodide en naftaleen?
Wat is het verschil smeltpunt van natriumjodide en naftaleen?  Hoe kun je aan de zuurstofbehoefte komen?
Hoe kun je aan de zuurstofbehoefte komen?  Magnetische T-Budbots gemaakt van theeplanten doden en reinigen biofilms
Magnetische T-Budbots gemaakt van theeplanten doden en reinigen biofilms Wat zijn materialen die het licht verzenden en verspreiden?
Wat zijn materialen die het licht verzenden en verspreiden?  Chemische evolutie:hoe leven voortkwam uit niet-levende materie
Chemische evolutie:hoe leven voortkwam uit niet-levende materie
 Degradatie van permafrost beïnvloedt hydrologische factoren in het brongebied van de Gele Rivier
Degradatie van permafrost beïnvloedt hydrologische factoren in het brongebied van de Gele Rivier NASA ziet sterke stormen in het ontwikkelen van golfsysteem 91L
NASA ziet sterke stormen in het ontwikkelen van golfsysteem 91L Is het moeilijk om bepaalde wetenschappelijke ontdekkingen te verdedigen in het Hof van de publieke opinie?
Is het moeilijk om bepaalde wetenschappelijke ontdekkingen te verdedigen in het Hof van de publieke opinie?  Hoe leggen slangen eieren?
Hoe leggen slangen eieren?  Nieuw-Zeeland lanceert plan om de gezondheid van meren en rivieren nieuw leven in te blazen
Nieuw-Zeeland lanceert plan om de gezondheid van meren en rivieren nieuw leven in te blazen
Hoofdlijnen
- Bosbessen en hun bestuivers komen niet van nature voor in Zuid-Afrika, maar lokale honingbijen kunnen helpen
- Welk type organisme gebruikt en produceert zowel zuurstofkoolstofdioxide?
- Welke cel passeert genetische informatie van de ene generatie tot de volgende generatie?
- Is een plantencel dood of levend?
- Wat is de volgorde van mRNA gemaakt van gen aaacaggtccca?
- Wat betekent anatomische structuren in een wetenschappelijke term?
- Wat is de intermembrale index van de mens?
- Hoe een microscoop te gebruiken om cellen te zien
- Waarom zou DNA, toen het zich eenmaal had ontwikkeld, het belangrijkste middel zijn geworden om genetische informatie over te dragen?
- Nieuw membraanwaterbehandelingssysteem om giftig afval en afvalverwerkingskosten met meer dan 90 procent te verminderen

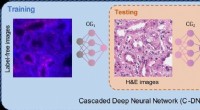
- Chemische vrije kleuring van weefsel met behulp van deep learning
- Video:Chemtrails versus contrails

- Zeemosselen zijn een model voor het verbeteren van kracht, rekbaarheid en hechting in hydrogels voor wondgenezing

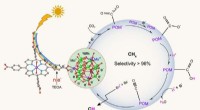
- Op polyoxometalaat gebaseerde coördinatiekaders voor de vorming van methaan bij de fotoreductie van koolstofdioxide
 Deze transformerende rover kan het moeilijkste terrein verkennen
Deze transformerende rover kan het moeilijkste terrein verkennen Hebben elanden ivoren tanden?
Hebben elanden ivoren tanden?  Onderzoek toont aan dat Vikingen genoten van een warmer Groenland
Onderzoek toont aan dat Vikingen genoten van een warmer Groenland Welke laag van de aarde is onderverdeeld in seprate -secties die platen worden genoemd?
Welke laag van de aarde is onderverdeeld in seprate -secties die platen worden genoemd?  Nieuwe innovatieve statistische tool verbetert de bestrijding van vervuiling in steden
Nieuwe innovatieve statistische tool verbetert de bestrijding van vervuiling in steden Veldstudie toont aan dat arseen in grondwater de rijstopbrengst in Bangladesh verlaagt
Veldstudie toont aan dat arseen in grondwater de rijstopbrengst in Bangladesh verlaagt Afbeelding:Straat Clarence, Australië
Afbeelding:Straat Clarence, Australië Geef een voorbeeld van bewijs van landkenmerken die het Wegeners -idee -continetal -drift ondersteunden?
Geef een voorbeeld van bewijs van landkenmerken die het Wegeners -idee -continetal -drift ondersteunden?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

