
Wetenschap
Inzicht in de pH:de schaal van zuurgraad en alkaliteit in de chemie
Door Robert Boumis – Bijgewerkt op 30 augustus 2022
De pH-schaal kwantificeert hoe zuur of basisch een stof is, een hoeksteenconcept in de scheikunde, biologie, geologie en veel toegepaste wetenschappen. Dankzij de beheersing van de pH kunnen wetenschappers kritische eigenschappen van materialen nauwkeurig communiceren.
Wat is pH?
pH, altijd in kleine letters geschreven, meet de concentratie waterstofionen (H⁺) in een oplossing. De schaal loopt van 0 tot 14, waarbij 7 staat voor neutraal, zuiver water. Waarden onder de 7 duiden op een toenemende zuurgraad, terwijl waarden boven de 7 een toenemende alkaliteit aangeven. Extreem zure of basische oplossingen kunnen corrosief zijn.
De schaal is logaritmisch, wat betekent dat elke eenheidsverandering overeenkomt met een tienvoudig verschil in waterstofionenconcentratie. Een oplossing met een pH van 4 bevat bijvoorbeeld tien keer meer H⁺ dan een oplossing met een pH van 5.
PH berekenen
Wiskundig gezien wordt de pH gedefinieerd als de negatieve logaritme met grondtal 10 van de waterstofionenconcentratie (uitgedrukt in mol per liter, of molariteit):
pH =–log₁₀[H⁺]
Deze conversie vereenvoudigt de weergave van waterstofionniveaus, waardoor het gemakkelijker wordt om oplossingen te vergelijken.
Praktisch voorbeeld
Stel dat u 1 liter oplossing heeft die 0,02 g waterstof bevat. Aangezien één mol waterstof ongeveer 1 g bedraagt, is de molariteit 0,02 molL⁻¹ (of 2×10⁻²M). Het nemen van de negatieve log geeft:
pH =–log₁₀(2×10⁻²) ≈ 1,7 (voor de eenvoud afgerond op 2). De oplossing is dus sterk zuur.
De pH bepalen op basis van pOH
pOH, de negatieve log van de hydroxide-ionenconcentratie, biedt een indirecte route naar de pH:
pOH =–log₁₀[OH⁻]
Omdat [H⁺][OH⁻] =1×10⁻¹⁴ bij 25°C, zijn pH en pOH gerelateerd door:
pH + pOH =14 → pH =14 – pOH
Een pOH van 12 levert bijvoorbeeld een pH van 2 op. De omgekeerde berekening gebruikt 14 – pH =pOH.
 Hoe wordt de atmosfeer vervuild?
Hoe wordt de atmosfeer vervuild?  Wat is de chemische samenstelling van kf-reagens?
Wat is de chemische samenstelling van kf-reagens?  Welke van de volgende beschrijft wat er gebeurt als ijzer (Fe) wordt geoxideerd tot Fe2-ionen?
Welke van de volgende beschrijft wat er gebeurt als ijzer (Fe) wordt geoxideerd tot Fe2-ionen?  Metalen beïnvloeden C-peptidehormoon gerelateerd aan insuline
Metalen beïnvloeden C-peptidehormoon gerelateerd aan insuline Zelfvoorzienende lus van chemische reacties kan een revolutie teweegbrengen in de productie van geneesmiddelen
Zelfvoorzienende lus van chemische reacties kan een revolutie teweegbrengen in de productie van geneesmiddelen
 Wat is het verschil tussen een microhabitat en bioom?
Wat is het verschil tussen een microhabitat en bioom?  De levenscyclus van grizzlyberen
De levenscyclus van grizzlyberen  Wat zijn de gevaren van zonnestralen door sneeuw?
Wat zijn de gevaren van zonnestralen door sneeuw?  Big data en machine learning inzetten om bosbranden in het westen van de VS te voorspellen
Big data en machine learning inzetten om bosbranden in het westen van de VS te voorspellen Verontreinigingsrisico van grondwater in karstregio's is hoger dan eerder werd aangenomen
Verontreinigingsrisico van grondwater in karstregio's is hoger dan eerder werd aangenomen
Hoofdlijnen
- Wat is het verschil tussen dominant en recessief gen?
- Wat is het verschil tussen planten- en dierencel?
- Wat zijn de problemen in verband met biotechnologie?
- Wat moet elke cel hebben?
- Zijn enzymen voornamelijk samengesteld uit eiwitten?
- Wat is een kolom in de wetenschap?
- Kan iemand zich herinneren dat hij geboren is?
- Wat is een voorbeeld van een kanaaleiwit?
- Waarom waren de S -bacteriën niet virulent?
- Onderzoek zoomt in op enzym dat DNA-schade door UV-stralen herstelt

- Moleculaire structuur van anti-verouderingseiwit alfa Klothos onthuld

- Wetenschappers hebben eiwitten gemaakt die worden gecontroleerd door licht
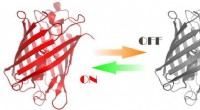
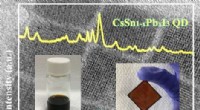
- Onderzoekers rapporteren fasestabiel anorganisch halide perovskiet
- Niet-gechloreerde, met oplosmiddel verwerkte hoogwaardige ambipolaire transistors

 Wat is de functie van transportweefsels in planten?
Wat is de functie van transportweefsels in planten?  Testen van ontworpen koolstofmaterialen om afvalwater te zuiveren
Testen van ontworpen koolstofmaterialen om afvalwater te zuiveren Hoeveel mol zuurstofatomen zijn aanwezig in 5.00 mol difosfor pentoxide P2O5?
Hoeveel mol zuurstofatomen zijn aanwezig in 5.00 mol difosfor pentoxide P2O5?  Wat Big Oil naar eigen zeggen wist over klimaatverandering
Wat Big Oil naar eigen zeggen wist over klimaatverandering Hoe keert u de dehydratatie -synthese om?
Hoe keert u de dehydratatie -synthese om?  What Is Low Density?
What Is Low Density?  Kun je me een zin geven met het woord fysieke wetenschap?
Kun je me een zin geven met het woord fysieke wetenschap?  Is de energie die in discrete pakketten komt?
Is de energie die in discrete pakketten komt?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

