
Wetenschap
Berekening van het massapercentage watervrij kopersulfaat in CuSO4·5H2O
Door Jack Brubaker
Bijgewerkt op 30 augustus 2022
Kopersulfaatpentahydraat (CuSO4·5H2O) is een hydraat, wat betekent dat de watermoleculen chemisch gebonden zijn aan het watervrije zout. Een monster van 100 gram van het hydraat bevat dus zowel kopersulfaat als water. Om uit te drukken hoeveel kopersulfaat er aanwezig is, gebruiken scheikundigen het massapercentage (massaprocent) van de watervrije component.
Stap 1 – Bepaal het formulegewicht van CuSO4·5H2O
Bereken met behulp van standaard atoomgewichten (IUPAC) de massa van elk element in de formule en tel deze op:
- Cu = 63,55amu × 1 = 63,55amu
- S = 32.07amu × 1 = 32.07amu
- O = 16.00amu × 9 = 144.00amu
- H = 1,01amu × 10 = 10,10amu
Formulegewicht = 63,55 + 32,07 + 144,00 + 10,10 = 249,72amu.
Stap 2 – Bepaal het formulegewicht van watervrij CuSO4
Verwijder de waterbijdrage:
- Cu = 63,55amu × 1 = 63,55amu
- S = 32.07amu × 1 = 32.07amu
- O = 16.00 uur × 4 = 64.00 uur
Formulegewicht = 63,55 + 32,07 + 64,00 = 159,62amu.
Stap 3 – Bereken het massapercentage CuSO4
Deel het watervrije gewicht door het hydraatgewicht en vermenigvuldig dit met 100%:
159,62/249,72 × 100 ≈ 63,92%
Een monster van 100 gram kopersulfaatpentahydraat bevat dus ongeveer 63,92 g CuSO4 en 36,08 g water.
Benodigde materialen
- Periodiek systeem der elementen
- Wetenschappelijke rekenmachine
TL;DR
Gebruik de atoomgewichten om de formulegewichten van CuSO4·5H2O en CuSO4 te berekenen, deel en vermenigvuldig vervolgens met 100 om het massapercentage watervrij kopersulfaat te verkrijgen (≈63,9%).
 Hoe te weten of een verbinding polair of niet-polair is?
Hoe te weten of een verbinding polair of niet-polair is?  Zwaveldioxideproductie door verbranding van koolwaterstofbrandstoffen:een chemische verklaring
Zwaveldioxideproductie door verbranding van koolwaterstofbrandstoffen:een chemische verklaring  Continu ademend metaal-organisch raamwerk met gastselectiviteit
Continu ademend metaal-organisch raamwerk met gastselectiviteit Nieuwe tijdsopgeloste ultraviolette fotodissociatie-massaspectrometriestrategie voor analyse van de stabiliteit van doeleiwitten
Nieuwe tijdsopgeloste ultraviolette fotodissociatie-massaspectrometriestrategie voor analyse van de stabiliteit van doeleiwitten  Onderzoekers leggen in realtime rondzwervende moleculaire fragmenten vast
Onderzoekers leggen in realtime rondzwervende moleculaire fragmenten vast
Hoofdlijnen
- Hoe watervlooien zich verdedigen tegen vleesetende planten
- Wat zijn alle factoren die de enzymactiviteit beïnvloeden, behalve voor temperatuur en pH?
- Welke fase van de celcyclus groeit een volledige grootte?
- Waarom evolueerden mensen maar wangen?
- Waar bevindt het jejunum zich in het menselijk lichaam?
- Wat is het verschil tussen plantencellen en dierencellen?
- Welke mutatie beïnvloedt een nakomelingen?
- Heeft een hybride allel er maar één voor eigenschap?
- Hoe verschilt celdeling tussen dier- en plantencellen?
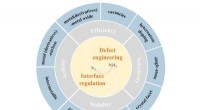
- Defect- en interface-engineering voor e-NRR onder omgevingsomstandigheden
- Rheostat geïdentificeerd die helpt bij het reguleren van celdood versus overlevingsbeslissingen

- Polymeren springen door hoepels op weg naar duurzame materialen

- Belangrijkste overeenkomsten tussen metalen en niet-metalen

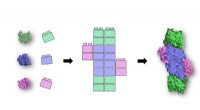
- Legos of life:een diepe duik in de 3D-structuren van eiwitten onthult belangrijke bouwstenen
 Waarom is veel kookpan gemaakt van aluminium, hoewel het een reactief metaal?
Waarom is veel kookpan gemaakt van aluminium, hoewel het een reactief metaal?  Wat is -40 graden Fahrenheit in Fahrenheit?
Wat is -40 graden Fahrenheit in Fahrenheit?  Waarom is het Easer om de beweging van N object te veranderen met een grote massa dan een object met kleinere massa?
Waarom is het Easer om de beweging van N object te veranderen met een grote massa dan een object met kleinere massa?  Welke lading heeft een elektron?
Welke lading heeft een elektron?  Wat zijn de termen voor een wasachtige of olieachtige organische verbinding?
Wat zijn de termen voor een wasachtige of olieachtige organische verbinding?  Wat gebeurt er met het oxidatie nummer wanneer een atoom in een reactant elektronen verliest?
Wat gebeurt er met het oxidatie nummer wanneer een atoom in een reactant elektronen verliest?
Het oxidatiegetal van een element geeft de hypothetische lading van een atoom in een verbinding aan. Het is hypothetisch omdat in de context van een verbi
 Bedankt, statistieken! Een snellere manier om mobiele apps te verbeteren
Bedankt, statistieken! Een snellere manier om mobiele apps te verbeteren Als een ster begint te vormen, is de initiële energiebron vorm?
Als een ster begint te vormen, is de initiële energiebron vorm?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

