
Wetenschap
Hoe gebogen moleculaire geometrieën te identificeren met behulp van VSEPR
Door Scott Becker
Bijgewerkt op 30 augustus 2022
De moleculaire vorm kan worden voorspeld met het Valence Shell Electron Pair Repulsion (VSEPR)-model, een fundamenteel hulpmiddel dat wordt onderwezen in geavanceerde scheikundecursussen over de hele wereld. VSEPR houdt rekening met het aantal bindingsplaatsen en alleenstaande paren rond een centraal atoom om de geometrie van een molecuul te voorspellen. Een “gebogen” vorm ontstaat wanneer een centraal atoom twee bindingsplaatsen en één of twee alleenstaande paren heeft. Door de principes van VSEPR toe te passen, kun je betrouwbaar bepalen of een molecuul een gebogen configuratie aanneemt.
Stap 1
Schrijf de chemische formule van het molecuul op (bijvoorbeeld HF, NO).
Stap 2
Bereken de totale valentie-elektronen met behulp van het periodiek systeem. Raadpleeg voor richtlijnen het gedeelte Bronnen over het tellen van elektronen.
Stap 3
Teken de Lewis-structuur:gebruik enkele lijnen voor bindingen en punten voor alleenstaande elektronen. Onthoud dat elke binding twee elektronen bijdraagt, en dat het totale aantal elektronen in de structuur gelijk moet zijn aan het aantal uit stap 2.
Stap 4
Identificeer het centrale atoom en tel de bindingsplaatsen plus de afzonderlijke elektronenparen. Dit is het sterische getal.
Stap 5
Analyseer het sterische getal:een gebogen geometrie vereist een sterisch getal van 3 of 4 met ten minste één vrijstaand paar. Als het getal verschilt, is het molecuul niet gebogen.
Stap 6
Raadpleeg een VSEPR-grafiek (zie bronnen) om het sterische getal, de bindingsplaatsen en de alleenstaande paren te matchen met de voorspelde moleculaire vorm.
TL;DR (te lang; niet gelezen)
Als bij het tekenen van de Lewis-structuur het aantal elektronen niet klopt, kunt u dit aanpassen door indien nodig dubbele of drievoudige bindingen toe te voegen en alleenstaande paren te verwijderen om een evenwichtige structuur te bereiken.
 Kan er een binding zijn tussen stikstof en zuurstof?
Kan er een binding zijn tussen stikstof en zuurstof?  Een revolutie in kunststoffen:het upcyclen van landbouwafval verhoogt de prestaties en duurzaamheid
Een revolutie in kunststoffen:het upcyclen van landbouwafval verhoogt de prestaties en duurzaamheid  Wat zijn enkele interessante ideeën voor chemieproject?
Wat zijn enkele interessante ideeën voor chemieproject?  Welk molecuul werd geproduceerd door de Elodea terwijl deze werd blootgesteld aan licht?
Welk molecuul werd geproduceerd door de Elodea terwijl deze werd blootgesteld aan licht?  Hoe maak je uit 37 procent HCL 0,5M HCL?
Hoe maak je uit 37 procent HCL 0,5M HCL?
 Wat eet of doodt een Tasmaanse duivel?
Wat eet of doodt een Tasmaanse duivel?  Voors en tegens van Styrofoam
Voors en tegens van Styrofoam Opwarmende temperaturen kunnen leiden tot hongersnood, uitsterven in diepe oceanen
Opwarmende temperaturen kunnen leiden tot hongersnood, uitsterven in diepe oceanen Tektonische platen zwakker dan eerder gedacht, zeggen wetenschappers
Tektonische platen zwakker dan eerder gedacht, zeggen wetenschappers Waarom water en voedingsstoffen geabsorbeerd door reizen naar de stengels bladeren?
Waarom water en voedingsstoffen geabsorbeerd door reizen naar de stengels bladeren?
Hoofdlijnen
- Het deel van de cel dat reguleert wat kan binnenkomen en vertrekken?
- Beoordeling van op SERS gebaseerde sensoren voor landbouwtoepassingen
- Wat is de oriëntatie van twee nucleotide -strengen in relatie tot elkaar?
- Waarom is Turgor -druk geen kenmerk van dierlijke cellen?
- Wat is verantwoordelijk voor het coderen van de eiwitten die in een cel worden gevonden?
- Zijn enzymen slechts een kleine minderheid van cellulaire massa uit?
- De schimmels onder zijn de grote ontbinders
- Hoe bioinformatica gerelateerd aan agrarische biotechnologie?
- Wat is een volledig levend materiaal rond de kern?
- Intelligent balsahout terugwinnen en recyclen

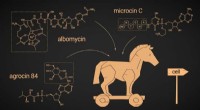
- Pas op voor mede-bacteriën die geschenken dragen:onderzoek presenteert nieuwe potentiële antimicrobiële middelen
- Nieuw concept voor het identificeren van chemische combinaties met mogelijke gezondheidseffecten

- Colloïdale gels, alomtegenwoordig in alledaagse producten, hun geheimen prijsgeven
- Leveren van hoogwaardige kankerbeeldvormende isotopen

 Mysterieuze gaten in Antarctisch zee-ijs verklaard door jarenlange robotgegevens
Mysterieuze gaten in Antarctisch zee-ijs verklaard door jarenlange robotgegevens Hoeveel energie is er nodig in Joules voor een vrouw van 90 kg was om ladder van 6 meter hoogte te beklimmen?
Hoeveel energie is er nodig in Joules voor een vrouw van 90 kg was om ladder van 6 meter hoogte te beklimmen?  Broom en natrium Een broomatoom krijgt een elektron en vormt het bromide-ion Br ndash. Wat gebeurt er met broom?
Broom en natrium Een broomatoom krijgt een elektron en vormt het bromide-ion Br ndash. Wat gebeurt er met broom?  Wetenschappers ontwikkelen een nieuw model om te beschrijven hoe bacteriën zich in verschillende vormen verspreiden
Wetenschappers ontwikkelen een nieuw model om te beschrijven hoe bacteriën zich in verschillende vormen verspreiden  Monitoring van de dynamiek van duizenden eiwitcomplexen tegelijk in intacte cellen
Monitoring van de dynamiek van duizenden eiwitcomplexen tegelijk in intacte cellen Archeologen graven een oude faraonische stad in Egypte op
Archeologen graven een oude faraonische stad in Egypte op Een vorm van energie die warmtelichtmagnetisme en elektrische ladingen kan produceren?
Een vorm van energie die warmtelichtmagnetisme en elektrische ladingen kan produceren?  Welke krachten bouwen bergen op?
Welke krachten bouwen bergen op?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

