
Wetenschap
Hoe u gemorst zoutzuur veilig kunt neutraliseren
Klaus Vedfelt/Getty Images
Zoutzuur, ook bekend als zoutzuur (HCl), is een veel voorkomende industriële en huishoudelijke chemische stof. Zelfs in verdunde vorm kan het de ogen, huid en luchtwegen irriteren, terwijl geconcentreerde oplossingen een ernstig risico op chemische brandwonden en, in extreme gevallen, de dood met zich meebrengen. Een snelle neutralisatie is essentieel om mens en milieu te beschermen.
Chemische reacties
Het neutraliseren van een zuur betekent het laten reageren met een base om een zout en water te produceren. De meest eenvoudige reactie maakt gebruik van natriumhydroxide (bijtende soda):
HCl + NaOH → NaCl + H₂O
Voor minder agressieve basen zoals zuiveringszout (natriumbicarbonaat), natriumcarbonaat (natriumcarbonaat) of kalk (calciumcarbonaat) komt bij de reactie kooldioxidegas vrij:
HCl + NaHCO₃ → NaCl + CO₂ + H₂O
Deze reacties combineren de waterstofionen van het zuur met de hydroxyl- of carbonaationen van de base, waardoor onschadelijk zout, water en, indien van toepassing, CO₂ ontstaan.
Hitte door chemische reacties
Zuur-base-neutralisatie is exotherm en kan aanzienlijke warmte genereren. Door snel mengen kan water verdampen en komt CO₂ vrij, wat de ogen en keel irriteert. Om de reactie onder controle te houden, voegt u de basis langzaam en in kleine stappen toe, zodat de warmte geleidelijk kan ontsnappen.
Beschermende kleding
Draag naast oogbescherming zuurbestendige handschoenen (neopreen of nitril). Latexhandschoenen zijn niet geschikt omdat deze oplossen in zuur. Houd alle ontstekingsbronnen uit de buurt van het werkgebied om brandrisico's te voorkomen.
Kleine lekkages
Voor lekkages in huis of in laboratoria zijn zuiveringszout, natriumcarbonaat of kalk de veiligste en meest economische neutralisatiemiddelen. Strooi de neutralisator rond de omtrek van de lekkage en werk naar binnen om schuimvorming te minimaliseren. Zodra het zuur is geneutraliseerd, bedek het gebied met droog zand, aarde of inert materiaal zoals vermiculiet, breng het residu over naar een daarvoor bestemde container voor chemisch afval en voer het af volgens de plaatselijke regelgeving.
Grote lekkages
In natuurlijke waterlopen of industriële omgevingen wordt gewoonlijk kalksteen of dolomiet (calcium-magnesiumcarbonaat) gebruikt om grote hoeveelheden zoutzuur te neutraliseren. Deze materialen reageren gedurende ongeveer 15 minuten en vormen een met zout beladen slib dat kan worden opgevangen en verwijderd. Kalksteen heeft over het algemeen de voorkeur vanwege zijn superieure reactiviteit en beschikbaarheid.
 Snelle weersschommelingen verhogen het risico op griep
Snelle weersschommelingen verhogen het risico op griep Welke soorten bacteriën produceren endosporen?
Welke soorten bacteriën produceren endosporen?  Waarom zijn deze attitudes belangrijk in de studie en de praktijk van de wetenschap?
Waarom zijn deze attitudes belangrijk in de studie en de praktijk van de wetenschap?  Australische toeristenindustrie onder bedreiging van klimaatverandering:studie
Australische toeristenindustrie onder bedreiging van klimaatverandering:studie Studie onthult hoe de aardgasproductie in schalie kan worden verbeterd
Studie onthult hoe de aardgasproductie in schalie kan worden verbeterd
Hoofdlijnen
- Wat zijn twee klieren die zijn afgeleid van neuraal weefsel?
- Welke organel is een kleine cirkelvormige en bevat enzymen?
- Fenotype:genexpressie en waarneembare eigenschappen begrijpen
- Welke actie zijn DNA -segmenten en bacteriën vergezeld?
- Wat zijn de voor- en nadelen van bio -energie?
- Wat is chemiosmose en wat zijn rol in cellulaire ademhaling?
- Wat is een andere naam voor het DNA -materiaal dat zich binnen de kern van een cel bevindt?
- AI-tool herkent ernstige oogziekten bij paarden
- Waarom veroorzaken levende bacteriën in voedselproducten zoals yoghurt geen ziekte van ziekten?
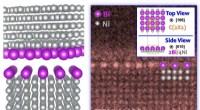
- besteld, door segregatie geïnduceerde bovenbouw aan algemene korrelgrenzen
- 3D-geprint materiaal ter vervanging van ivoor voor restauratie van artefacten

- Middeleeuwse blauwe kleurstoffen moleculaire structuur geïdentificeerd

- De olie uit vervuild water halen

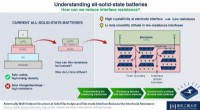
- Glashelder maken:kristalliniteit vermindert de weerstand in volledig solid-state batterijen
 Wat gebeurt er met de lichtstraal als het water raakt?
Wat gebeurt er met de lichtstraal als het water raakt?  Onderzoekers identificeren virusresistentiegen van wild gras voor verbetering van graangewassen
Onderzoekers identificeren virusresistentiegen van wild gras voor verbetering van graangewassen Giftige, brandwerende chemicaliën kunnen worden geabsorbeerd door aanraking, zo blijkt uit een 3D-geprint huidmodel
Giftige, brandwerende chemicaliën kunnen worden geabsorbeerd door aanraking, zo blijkt uit een 3D-geprint huidmodel  Kan AI de verspreiding van HIV onder dakloze jongeren voorkomen?
Kan AI de verspreiding van HIV onder dakloze jongeren voorkomen?  LPG en biogas:de voordelen van schonere brandstoffen begrijpen
LPG en biogas:de voordelen van schonere brandstoffen begrijpen  Hoe bereid je je voor op een hyperactief orkaanseizoen
Hoe bereid je je voor op een hyperactief orkaanseizoen Hoe noem je elementen die niet op natuurlijke wijze bestaan?
Hoe noem je elementen die niet op natuurlijke wijze bestaan?  India's geïntegreerde programma voor de ontwikkeling van kinderen verhoogt het opleidingsniveau
India's geïntegreerde programma voor de ontwikkeling van kinderen verhoogt het opleidingsniveau
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

