
Wetenschap
Zuurstofsmeltpunt:sublimatie en faseovergangen begrijpen
* Zuurstof is een gas bij kamertemperatuur en druk. Het moet aanzienlijk worden afgekoeld voordat het vloeibaar wordt en vervolgens nog verder om vast te worden.
* Het "smeltpunt" van zuurstof is de temperatuur waarbij het overgaat van vast naar vloeibaar. Zuurstof gaat echter direct over van een gas naar een vaste stof (en omgekeerd) bij standaard atmosferische druk. Dit wordt sublimatie genoemd .
* Het "triple punt" van zuurstof is de temperatuur en druk waarbij alle drie de fasen (vast, vloeibaar en gas) in evenwicht naast elkaar bestaan. Voor zuurstof ligt dit punt op -218,79°C (-361,82°F) en 0,0015 atmosfeer.
Dus hoewel zuurstof geen traditioneel smeltpunt heeft, heeft het wel een tripelpunt.
 Nieuwe wetenschappelijke methode om waterkwaliteitscriteria van metalen af te leiden voor de bescherming van verschillende mariene ecosystemen wereldwijd
Nieuwe wetenschappelijke methode om waterkwaliteitscriteria van metalen af te leiden voor de bescherming van verschillende mariene ecosystemen wereldwijd Hoe je spanning omzet in transformatie
Hoe je spanning omzet in transformatie Nieuwe tool onthult de echte broeikasgasvoetafdruk van reservoirs
Nieuwe tool onthult de echte broeikasgasvoetafdruk van reservoirs LC50-waarden berekenen
LC50-waarden berekenen  Wat staat er op YouTube? 'YouTube Nation' laat het je weten
Wat staat er op YouTube? 'YouTube Nation' laat het je weten
Hoofdlijnen
- Gepersonaliseerde faagtherapie geneest resistente wonden bij Siamese katten
- Hoe worden de kleine strengen die in een cel genoemd?
- Australisch onderzoek bewijst dat mensen het meest angstaanjagende roofdier van de planeet zijn
- Behandeling van antibioticaresistente infecties met peptiden geïnspireerd op menselijk speeksel
- Welk proces produceert een exacte kopie van het ouderorganisme?
- Wat is het debat tussen evolutiebiologie en creationisme?
- Nuclear DNA:Structure, Location &Function - A Comprehensive Guide
- Wat betekent het dat een cel onsterfelijk is?
- Welke manier groeperen wetenschappers organismen?
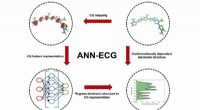
- Nieuwe benadering van moleculaire modellering kan de ontwikkeling van nieuwe organische materialen voor elektronica versnellen
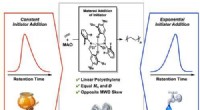
- Afdrukbaar, kleurrijke camouflage met polymeren

- Op Mars of de aarde, biohybride kan koolstofdioxide omzetten in nieuwe producten

- Diepeutectische oplosmiddelen vervangen vervuilende industriële oplosmiddelen

- Triangle 2 plastic containers kunnen een make-over voor het milieu ondergaan
 Wanneer een geladen deeltje wordt verplaatst langs een elektrische veldlijn?
Wanneer een geladen deeltje wordt verplaatst langs een elektrische veldlijn?  Rapport identificeert factoren die verband houden met intimidatie, misbruik in academisch veldwerk
Rapport identificeert factoren die verband houden met intimidatie, misbruik in academisch veldwerk Klimaatverandering maakt bouwen, visserij en andere gevaarlijke industrieën nog riskanter
Klimaatverandering maakt bouwen, visserij en andere gevaarlijke industrieën nog riskanter Wat is een reden dat ozon in de buurt van het Superface gevaarlijk is?
Wat is een reden dat ozon in de buurt van het Superface gevaarlijk is?  Tropische cyclonen in de Arabische Zee:waarom nemen ze toe?
Tropische cyclonen in de Arabische Zee:waarom nemen ze toe?  In welke richting werkt wrijvingshandeling vergeleken o de beweging?
In welke richting werkt wrijvingshandeling vergeleken o de beweging?  ATP:de energievaluta van cellen - Synthese en cellulaire processen
ATP:de energievaluta van cellen - Synthese en cellulaire processen  Draagbaar biomedisch apparaat op basis van grafeen om diabetes te monitoren en te bestrijden
Draagbaar biomedisch apparaat op basis van grafeen om diabetes te monitoren en te bestrijden
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

