
Wetenschap
Elektronegativiteit en bindingstype:inzicht in ionische versus covalente bindingen
1. Elektronegativiteit:een maatstaf voor de aantrekkingskracht van een atoom op elektronen
Elektronegativiteit is een eigenschap van een atoom die de neiging beschrijft om elektronen naar zichzelf toe te trekken wanneer het een chemische binding vormt. Hoe hoger de elektronegativiteitswaarde van een atoom, hoe sterker de aantrekkingskracht op gedeelde elektronen.
2. Het verschil in elektronegativiteit bepaalt het bindingstype:
* Ionische bindingen: Wanneer het verschil in elektronegativiteit tussen twee atomen groot is (doorgaans groter dan 1,7), zal één atoom een veel sterkere aantrekkingskracht uitoefenen op de gedeelde elektronen. Dit leidt tot de volledige overdracht van elektronen van het minder elektronegatieve atoom naar het meer elektronegatieve atoom, resulterend in de vorming van ionen (positief geladen kation en negatief geladen anion). Deze tegengesteld geladen ionen worden vervolgens bij elkaar gehouden door elektrostatische krachten, waardoor een ionische binding ontstaat.
* Covalente bindingen: Wanneer het verschil in elektronegativiteit klein is (doorgaans minder dan 1,7), heeft geen van beide atomen een significant sterkere aantrekkingskracht op de elektronen. Dit resulteert in het delen van elektronen tussen de atomen, waardoor een covalente binding ontstaat.
* Niet-polaire covalente bindingen: Als het elektronegativiteitsverschil erg klein of nul is (zoals bij een binding tussen twee identieke atomen), worden de elektronen gelijkelijk verdeeld tussen de atomen.
* Polaire covalente bindingen: Als het elektronegativiteitsverschil gematigd is, worden de elektronen ongelijk verdeeld, waardoor een gedeeltelijk positieve lading (δ+) ontstaat op het minder elektronegatieve atoom en een gedeeltelijk negatieve lading (δ-) op het meer elektronegatieve atoom. Deze ongelijke verdeling leidt tot een polaire covalente binding.
Samengevat:
* Groot elektronegativiteitsverschil =Ionische binding
* Klein elektronegativiteitsverschil =Covalente binding (kan niet-polair of polair zijn)
Voorbeeld:
* NaCl (natriumchloride): Natrium (Na) heeft een elektronegativiteit van 0,93, terwijl chloor (Cl) een elektronegativiteit van 3,16 heeft. Het verschil is groot (2,23), resulterend in de vorming van een ionische binding waarbij natrium een elektron verliest om een kation te worden (Na+) en chloor een elektron krijgt om een anion te worden (Cl-).
* H2O (water): Zuurstof (O) heeft een elektronegativiteit van 3,44, terwijl waterstof (H) een elektronegativiteit van 2,20 heeft. Het verschil is gematigd (1,24), wat leidt tot een polaire covalente binding waarbij zuurstof een gedeeltelijk negatieve lading heeft en waterstof een gedeeltelijk positieve lading.
Bedenk dat elektronegativiteit een nuttig hulpmiddel is voor het voorspellen van het karakter van bindingen, maar dat het niet de enige factor is. Andere factoren zoals de atoomgrootte en het aantal elektronenschillen kunnen ook het bindingstype beïnvloeden.
 Verouderde infrastructuur in Amerika zakt in onder de druk van klimaatverandering
Verouderde infrastructuur in Amerika zakt in onder de druk van klimaatverandering Diep boren naar aanwijzingen over aardbevingen
Diep boren naar aanwijzingen over aardbevingen Canadese energieregulator geeft knipoog naar Pacific-pijpleiding
Canadese energieregulator geeft knipoog naar Pacific-pijpleiding NASA ziet tropische storm Sonca aan land komen in Vietnam
NASA ziet tropische storm Sonca aan land komen in Vietnam India's vuurwerkcentrum getroffen door anti-vervuilingsactie
India's vuurwerkcentrum getroffen door anti-vervuilingsactie
Hoofdlijnen
- Welk type cellen omringen vasculair weefsel een plantenstam?
- Hoe brengen planten microbiële vrienden en vijanden in evenwicht?
- Belang van biotechnologie in je leven?
- Life Science staat ook bekend als?
- Verschuivende aanwezigheid van Noord-Atlantische walvissen gevolgd met passieve akoestiek
- Worden eiwitten getransporteerd door de Golgi -lichamen?
- Wat zijn drie levende voorbeelden van organismen?
- Wat zijn twee paar tegengestelde processen?
- Wat maakt het een uitdaging om genetisch materiaal in eukaryotische cellen te verpakken?
- Russische popmoleculen kunnen echt opruimen
- Nieuwe toepassingen vinden voor afvalbanden

- Wetenschappers ontwikkelen elastische metalen staven om scoliose te behandelen

- Dynamiek van massa-actie in niet-stabiele toestand heroverwogen
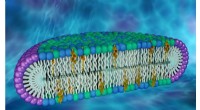
- Nieuw celmembraanmodel kan de sleutel zijn tot het ontdekken van nieuwe eiwiteigenschappen
 Video:studenten insectenbiologie leren kunst van op insecten gebaseerde kleurstoffen
Video:studenten insectenbiologie leren kunst van op insecten gebaseerde kleurstoffen Hoe krijgen bloemen hun voedsel?
Hoe krijgen bloemen hun voedsel?  Wat oorzaak van een zonne -halo?
Wat oorzaak van een zonne -halo?  Onderzoekers onderzoeken de correlatie tussen wind en golfhoogte in de Noordelijke IJszee
Onderzoekers onderzoeken de correlatie tussen wind en golfhoogte in de Noordelijke IJszee Wat is de tweede meest voorkomende vloeistof?
Wat is de tweede meest voorkomende vloeistof?  Hoe leer je High School Math Online
Hoe leer je High School Math Online Vraag ons ALLESOCTANE (C8H18) is te vinden in benzine. Het verbrandde voor brandstof een verbrandingsreactie. Het onevenwichtige reactie -octaan hieronder getoond. C8H18 plus O2 CO2 H2O warmte W?
Vraag ons ALLESOCTANE (C8H18) is te vinden in benzine. Het verbrandde voor brandstof een verbrandingsreactie. Het onevenwichtige reactie -octaan hieronder getoond. C8H18 plus O2 CO2 H2O warmte W?  Is kolen en aardgas hetzelfde?
Is kolen en aardgas hetzelfde?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

