
Wetenschap
Waterstofbruggen in water:hoe ze moleculen bij elkaar houden
Dit is waarom:
* Polariteit: Watermoleculen zijn polair, wat betekent dat ze een enigszins positief uiteinde (de waterstofatomen) en een enigszins negatief uiteinde (het zuurstofatoom) hebben.
* Attractie: Het enigszins positieve waterstofuiteinde van het ene watermolecuul wordt aangetrokken door het enigszins negatieve zuurstofuiteinde van een ander watermolecuul.
* Zwakke band: Deze aantrekkingskracht wordt een waterstofbrug genoemd en is een zwak type binding vergeleken met covalente bindingen.
Waterstofbruggen zijn cruciaal voor de eigenschappen van water, inclusief het hoge kookpunt, de oppervlaktespanning en het vermogen om als oplosmiddel te werken.
 Hoe zagen onze voorouders eruit?
Hoe zagen onze voorouders eruit?  Digitale landbouw effent de weg naar agrarische duurzaamheid
Digitale landbouw effent de weg naar agrarische duurzaamheid De blauwe economie is meer dan middelen:ze moet zich richten op sociale rechtvaardigheid en bestuur
De blauwe economie is meer dan middelen:ze moet zich richten op sociale rechtvaardigheid en bestuur The Antarctic:Study levert gegevens over de structuur van het ijzige continent
The Antarctic:Study levert gegevens over de structuur van het ijzige continent Nieuwe studieprojecten oceaanopwarming impact op Antarctische krill
Nieuwe studieprojecten oceaanopwarming impact op Antarctische krill
Hoofdlijnen
- Wat betekent de term RNP in de biologie?
- Gebruik je echt maar 10 procent van je hersenen?
- Bacteriële groei in petrischalen meten
- Hoe produceren organismen nieuwe cellen die exacte kopieën van de bestaande cellen zijn?
- Waar classificeren biologen in levende wezens bij betrokken?
- Waarom zijn nucleïnezuren belangrijk voor levende wezens?
- De Atlantische steuren verblijven
- Hoe grassen zoals tarwe in de kou kunnen groeien
- Een vasculaire plant die zich voortplant met sporen is een varen?
- Elektrische versus traditionele autobatterijen:belangrijkste verschillen verklaard

- Een nieuwe cermet die een betere warmte-uitwisseling voor zonne-energiecentrales zou kunnen bieden

- Onderzoekers ontwikkelen nieuwe meetmethode in moleculaire elektronica
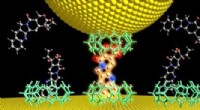
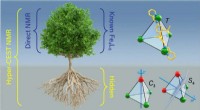
- Hyper-CEST NMR-techniek onthult ontbrekende structuur van een nieuw containermolecuul
- Dubbele vervangingsreacties uitgelegd:hoe ionen gassen uitwisselen, neerslaan of vormen

 Hebben alleen mensen energie nodig om te overleven?
Hebben alleen mensen energie nodig om te overleven?  Wat is de wetenschapsdefinitie voor Top Predator?
Wat is de wetenschapsdefinitie voor Top Predator?  Een frisse kijk op graslanden als koolstofputten
Een frisse kijk op graslanden als koolstofputten Welke wiskunde gebruikte Benjamin Banneker om zonne -advertenties voor zonne -AD te voorspellen?
Welke wiskunde gebruikte Benjamin Banneker om zonne -advertenties voor zonne -AD te voorspellen?  Hoe wordt het genoemd als de snelheid op een bepaald moment hetzelfde blijft?
Hoe wordt het genoemd als de snelheid op een bepaald moment hetzelfde blijft?  China's ruimtedroom:een lange mars naar de maan
China's ruimtedroom:een lange mars naar de maan Verschillen tussen een zure wasmiddelvezel en een neutrale detergent Fiber
Verschillen tussen een zure wasmiddelvezel en een neutrale detergent Fiber Paintball Science Fair Project Ideas
Paintball Science Fair Project Ideas
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

