
Wetenschap
Temperatuurverandering bij het oplossen van ammoniumchloride:een verklaring
Dit is waarom:
* Het oplossen van ammoniumchloride is endotherm: Het proces waarbij ammoniumchloride in water wordt opgelost, is een endotherme reactie. Dit betekent dat het warmte uit de omgeving absorbeert, waardoor de temperatuur van het water daalt.
* Verbindingen verbreken en vormen: Wanneer ammoniumchloride oplost, worden de ionische bindingen tussen de ammonium- (NH₄⁺) en chloride- (Cl⁻) ionen verbroken. Hiervoor is energie nodig, die uit het water wordt opgenomen. Tegelijkertijd worden er nieuwe bindingen gevormd tussen de ionen en watermoleculen (hydratatie), maar bij dit proces komt minder energie vrij dan er wordt geabsorbeerd bij het verbreken van de oorspronkelijke bindingen.
Samengevat: De totale energiebalans resulteert in een netto opname van warmte uit de omgeving, wat leidt tot een verlaging van de temperatuur van het water.
 Ouder, dichtere buurten bieden een betere toegang tot alledaagse bestemmingen, studie vondsten
Ouder, dichtere buurten bieden een betere toegang tot alledaagse bestemmingen, studie vondsten NASA ziet recordbrekende nieuwe tropische storm Gonzalo versterken
NASA ziet recordbrekende nieuwe tropische storm Gonzalo versterken De aardbeving van 2017 in Mexico kwam voort uit een groeiende risicozone
De aardbeving van 2017 in Mexico kwam voort uit een groeiende risicozone Degradatie van permafrost beïnvloedt hydrologische factoren in het brongebied van de Gele Rivier
Degradatie van permafrost beïnvloedt hydrologische factoren in het brongebied van de Gele Rivier Video:Waarom Antarctische vissen niet doodvriezen
Video:Waarom Antarctische vissen niet doodvriezen
Hoofdlijnen
- Waarom kippenvel er nog steeds toe doet:de verborgen rol van de Arrector Pili-spier
- Wat zijn de nadelen van een dierencel?
- Een nieuwe regulator van de handel in blaasjes in planten
- Wetenschappers publiceren nieuw onderzoek naar hoe individuele cellen reageren op virale infecties
- Cytoskelet:structuur, functie en belang in eukaryotische cellen
- Komt alle weefsels van dezelfde embryonale oorsprong?
- Welke activiteit zou op het gebied van biololgy zijn?
- Wat bepaalt welk bioom bestaat in een bepaald gebied?
- Waarom de stinkende durian echt 'koning van alle vruchten' is
- Onderzoekers creëren slimme oppervlakken om bloedvattransplantaten beter te laten breien, veiliger

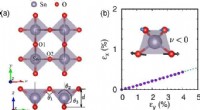
- Onderzoekers maken theoretische voorspelling van 2-D halfgeleider tindioxide
- Video:Eindelijk (peer-reviewed) chemie in wijn- en spijscombinaties

- Deze hydrogeltablet kan een liter rivierwater in een uur zuiveren

- Flexibele vaste elektrolyten voor all-solid-state lithiumbatterijen

 Wat zijn de voor- en nadelen van vleugelergie?
Wat zijn de voor- en nadelen van vleugelergie?  Wat is de orde van planeet uit de zon?
Wat is de orde van planeet uit de zon?  Kunnen honden snel woorden leren?
Kunnen honden snel woorden leren?  Dingen laten drijven in water
Dingen laten drijven in water Klimaatverandering om sommige Amerikaanse waterbassins uit te putten, de opbrengst van geïrrigeerde gewassen verminderen
Klimaatverandering om sommige Amerikaanse waterbassins uit te putten, de opbrengst van geïrrigeerde gewassen verminderen Kun je 5 inch converteren naar mm?
Kun je 5 inch converteren naar mm?  Wat zijn vijftien termen voor kernenergie?
Wat zijn vijftien termen voor kernenergie?  Jerry Nelson, astronoom die geavanceerde telescopen bouwde, overlijdt
Jerry Nelson, astronoom die geavanceerde telescopen bouwde, overlijdt
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

