
Wetenschap
Metaalkarakter van elementen:eigenschappen identificeren op het periodiek systeem
Metaalachtig karakter
* Definitie: Metallisch karakter verwijst naar hoe gemakkelijk een element elektronen verliest om positieve ionen (kationen) te vormen. Deze eigenschap neemt over het algemeen toe naarmate u naar beneden en naar links in het periodiek systeem beweegt.
* Belangrijkste factoren:
* Elektronegativiteit: Elementen met een lagere elektronegativiteit verliezen eerder elektronen (meer metallisch).
* Ionisatie-energie: Elementen met een lagere ionisatie-energie (gemakkelijker om elektronen te verwijderen) zijn meer metallisch.
* Atomische grootte: Bij grotere atomen bevinden de buitenste elektronen zich verder van de kern, waardoor ze gemakkelijker te verwijderen zijn (meer metallisch).
De 3e periode
De 3e periode van het periodiek systeem omvat elementen van natrium (Na) tot Argon (Ar). Naarmate u de periode van links naar rechts doorloopt, neemt het metaalachtige karakter af.
Elementen na de derde periode
De elementen *na* de 3e periode zouden zich in de 4e periode bevinden. Deze elementen zijn:
* Kalium (K)
* Calcium (Ca)
* Scandium (Sc)
* Titaan (Ti)
* Vanadium (V)
* Chroom (Cr)
* Mangaan (Mn)
* IJzer (Fe)
* Kobalt (Co)
* Nikkel (Ni)
* Koper (Cu)
* Zink (Zn)
* Gallium (Ga)
* Germanium (Ge)
* Arseen (As)
* Selenium (Se)
* Broom (Br)
* Krypton (Kr)
Het antwoord
Van deze elementen Kalium (K) zou het meest metaalachtige karakter hebben. Dit is waarom:
* Positie: Het staat in de eerste kolom (alkalimetalen), bekend om hun sterke metallische eigenschappen.
* Elektronegativiteit: Het heeft een zeer lage elektronegativiteit.
* Ionisatie-energie: Het heeft een relatief lage ionisatie-energie.
Belangrijke opmerking: Hoewel elementen verderop in de 4e periode (zoals Scandium en Titanium) ook metalen zijn, zal Kalium het meest metallisch zijn vanwege zijn positie op het periodiek systeem.
 Verschil tussen Nylon 6 en Nylon 66
Verschil tussen Nylon 6 en Nylon 66  Waarom is koolmonoxide giftig en kooldioxide niet?
Waarom is koolmonoxide giftig en kooldioxide niet?  Hoeveel mol N2 zijn er bij een temperatuur 20 graden Celsius 1 atm druk als het gas 44 liter bezet?
Hoeveel mol N2 zijn er bij een temperatuur 20 graden Celsius 1 atm druk als het gas 44 liter bezet?  Wat is een chemische vergelijking waarin zowel de reactant als het product een gelijk aantal atomen hebben bij een gegeven element?
Wat is een chemische vergelijking waarin zowel de reactant als het product een gelijk aantal atomen hebben bij een gegeven element?  Wat is het proces van warmteoverdracht door een metaal?
Wat is het proces van warmteoverdracht door een metaal?
 Hoe passen mensen zich aan aan hun omgeving?
Hoe passen mensen zich aan aan hun omgeving?  Ingenieurs schijnen licht op dodelijke aardverschuiving
Ingenieurs schijnen licht op dodelijke aardverschuiving Nieuwe studie onthult hoe ijzige oppervlaktevijvers op Himalaya-gletsjers de waterstroom beïnvloeden
Nieuwe studie onthult hoe ijzige oppervlaktevijvers op Himalaya-gletsjers de waterstroom beïnvloeden Welke planten zijn te vinden in Mt Rainier National Park?
Welke planten zijn te vinden in Mt Rainier National Park?  Wat is het proces waarmee individuen hun sensorische indrukken organiseren en interpreteren om betekenisomgeving te geven?
Wat is het proces waarmee individuen hun sensorische indrukken organiseren en interpreteren om betekenisomgeving te geven?
Hoofdlijnen
- Wat is de naam van enzym in speeksel en welke verbinding heeft geproduceerd als dit op zetmeel werkt?
- Wat is een veronderstelde ontwikkeling van het leven van de gewone voorouder?
- De activiteit van alle systemen voor het menselijk lichaam wordt gecoördineerd door wat?
- Wat betekent het als organismen evolueren?
- Hoe krijgen mensen stikstof in hun lichaam?
- Welke term wordt gebruikt om een dierengenen te beschrijven die zijn gewijzigd met behulp van biotechnologie?
- Bijtkrachtonderzoek onthult dinosaurus-etende kikker
- Veelhoekige cellen begrijpen:context en verduidelijking
- Een bioloog meet de allelfrequenties van erwtenplanten in een zeer gecontroleerde omgeving. Het kan dominante lange (t) of recessieve korte (t) hebben. Welke volgt?
- Structuur van elektrolyt regelt batterijprestaties
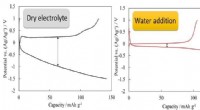
- Goedkope techniek voor het etsen van nanogaten in silicium zou de basis kunnen vormen voor nieuwe filtratie- en nanofotonische apparaten

- Onderzoekers melden doorbraak in 3D-geprint latexrubber

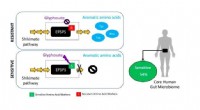
- Glyfosaat kan de menselijke darmflora beïnvloeden
- Honingraatstructuur met zuurstofarme poriën gevonden in oxideschaal op kleine, op lood gebaseerde reactormaterialen

 Wat is de uiteindelijke vorm van chemische energie geproduceerd door cellen tijdens cellulaire ademhaling?
Wat is de uiteindelijke vorm van chemische energie geproduceerd door cellen tijdens cellulaire ademhaling?  Hoe wetenschappers NASA-gegevens gebruikten om de corona van 21 augustus Total Solar Eclipse te voorspellen
Hoe wetenschappers NASA-gegevens gebruikten om de corona van 21 augustus Total Solar Eclipse te voorspellen  Hoe verschilt Aurora Borealis van Australis?
Hoe verschilt Aurora Borealis van Australis?  Kunnen protisten parasieten of ontleders zijn?
Kunnen protisten parasieten of ontleders zijn?  Is Tin een isolator of een geleider?
Is Tin een isolator of een geleider?  Hoe reageert SOAP met de zouten CACL2 of MGCL2?
Hoe reageert SOAP met de zouten CACL2 of MGCL2?  Hoe kun je zien of cellen in mitose dieren of plantencellen zijn?
Hoe kun je zien of cellen in mitose dieren of plantencellen zijn?  Wat is de grootste vlakte?
Wat is de grootste vlakte?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

