
Wetenschap
Ionisatie van niet-metalen:anionvorming begrijpen
* Niet-metalen hebben een hoge elektronegativiteit: Dit betekent dat ze een sterke aantrekkingskracht hebben op elektronen.
* Ze zijn meestal dichter bij een volledig octet: Niet-metalen hebben doorgaans een groter aantal valentie-elektronen (elektronen in de buitenste schil) vergeleken met metalen. Door elektronen te verkrijgen, kunnen ze een stabiele elektronenconfiguratie bereiken die lijkt op het dichtstbijzijnde edelgas.
Hier is een overzicht:
1. Elektronenversterking: Een niet-metaalatoom krijgt een of meer elektronen van een ander atoom.
2. Vorming van anion: Het atoom wordt negatief geladen omdat het nu meer elektronen dan protonen heeft.
3. Stabiele elektronenconfiguratie: Het anion bereikt een stabiele elektronenconfiguratie, vergelijkbaar met een edelgas.
Voorbeeld:
* Chloor (Cl), een niet-metaal, heeft 7 valentie-elektronen.
* Wanneer het één elektron krijgt, wordt het een chloride-ion (Cl⁻).
* Cl⁻ heeft nu 8 valentie-elektronen, vergelijkbaar met de stabiele elektronenconfiguratie van argon (Ar).
Belangrijke opmerkingen:
* Het aantal gewonnen elektronen hangt af van het specifieke niet-metaal. Zuurstof (O) krijgt bijvoorbeeld twee elektronen om het oxide-ion (O²⁻) te vormen.
* Het ionisatieproces gaat vaak gepaard met de vorming van ionische verbindingen. Dit gebeurt wanneer een metaalatoom elektronen verliest (waarbij een kation wordt gevormd) en een niet-metaalatoom elektronen wint (een anion vormt), wat resulteert in een elektrostatische aantrekkingskracht tussen hen.
Laat het me weten als je nog vragen hebt!
 Waarom moet water vloeistof worden genoemd?
Waarom moet water vloeistof worden genoemd?  Wat is de chemische formule van Fitkari?
Wat is de chemische formule van Fitkari?  De stabiliteit van de driedimensionale vorm is veel grote moleculen afhankelijk van?
De stabiliteit van de driedimensionale vorm is veel grote moleculen afhankelijk van?  Waarom blaast een atoom op als je het in tweeën splitst?
Waarom blaast een atoom op als je het in tweeën splitst?  Wat zou er gebeuren als je een universele indicatoroplossing aan water zou toevoegen als de reactie met kalium was afgelopen?
Wat zou er gebeuren als je een universele indicatoroplossing aan water zou toevoegen als de reactie met kalium was afgelopen?
 Kan alles in de dode zee leven?
Kan alles in de dode zee leven?  Wat zijn 4 voorbeelden van levende wezens?
Wat zijn 4 voorbeelden van levende wezens?  Wat is een groenblijvende boom met stekelige bladeren?
Wat is een groenblijvende boom met stekelige bladeren?  Deskundigen reageren op het laatste rapport van het Intergouvernementeel Panel over klimaatverandering
Deskundigen reageren op het laatste rapport van het Intergouvernementeel Panel over klimaatverandering Online calculator laat zien hoe bomen de luchtkwaliteit kunnen verbeteren en de gezondheidskosten kunnen verlagen
Online calculator laat zien hoe bomen de luchtkwaliteit kunnen verbeteren en de gezondheidskosten kunnen verlagen
Hoofdlijnen
- Wat stond wetenschappers in staat om met de celtheorie te komen?
- DNA-klonen: definitie, proces, voorbeelden
- Van groepsimmuniteit en zelfgenoegzaamheid tot groepspaniek:hoe vaccinatieangst zich ontvouwt
- Wat is het belang van eiwitten in de biologie?
- Een weefsel of structuur die zich superieur bevindt aan het hyoid bot Er zijn twee woorden in naam hiervan wat het is?
- Wat zijn de drie systemen waaruit vasculaire planten bestaat?
- Wat betekent bibiologie?
- Wat bedoel je met fotosynthese?
- Wat is een celorganel met de bijnaam krachtpatser?
- Een puzzel strijken

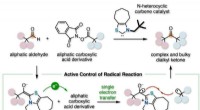
- Organokatalysator die radicale reacties regelt voor complexe en omvangrijke synthese van verbindingen
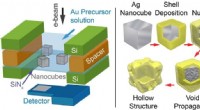
- Realtime beeldvorming van chemische processen
- Nanoporeuze materiaalnetten verontreinigende stoffen uit water

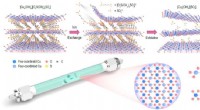
- Ultradun 2D cupraat met actieve periodieke koperen enkele sites, een nieuwe katalysator voor Chan-lam-koppeling
 Methode gebruikt om stoffen te scheiden vanwege verschillen in hun dichtheid?
Methode gebruikt om stoffen te scheiden vanwege verschillen in hun dichtheid?  Wat zijn beperkingen in de wetenschap?
Wat zijn beperkingen in de wetenschap?  Chengjian-fauna:evolutie van dieren en geboorte van fundamentele menselijke organen
Chengjian-fauna:evolutie van dieren en geboorte van fundamentele menselijke organen Wat is het meest voorkomende edelgas op periodieke tabel?
Wat is het meest voorkomende edelgas op periodieke tabel?  Welke cellen zijn lang en rechthoekig en hebben cilia?
Welke cellen zijn lang en rechthoekig en hebben cilia?  Hoe gedraagt ammoniumchloride zich in water?
Hoe gedraagt ammoniumchloride zich in water?  Waar is de bootle -steen op Walney Island Cumbria?
Waar is de bootle -steen op Walney Island Cumbria?  Welk type weefsel bedekt het lichaamsoppervlak en lijnen organen?
Welk type weefsel bedekt het lichaamsoppervlak en lijnen organen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

