
Wetenschap
Bariumchloridehydraat naar watervrij conversie:temperatuur en proces
* Bariumchloridedihydraat (BaCl₂·2H₂O): Dit is de meest voorkomende vorm van bariumchloride. Het is wit, kristallijn en bevat twee watermoleculen per formule-eenheid.
* Watervrij bariumchloride (BaCl₂): Deze vorm is ook wit en kristallijn, maar bevat geen watermoleculen.
Om bariumchloridedihydraat om te zetten in watervrij bariumchloride, moet je het verwarmen. De temperatuur die nodig is voor deze conversie is niet een specifiek enkel punt, maar eerder een bereik vanwege factoren zoals verwarmingssnelheid, druk en de specifieke vorm van het hydraat.
Hier is een algemene richtlijn:
* Uitdroging begint rond 100°C: Bij deze temperatuur begint het dihydraat zijn watermoleculen te verliezen.
* Volledige uitdroging rond 150°C: Bij deze temperatuur gaan de meeste watermoleculen verloren, waardoor je watervrij bariumchloride overhoudt.
* Verder verwarmen boven 150°C: Dit wordt niet aanbevolen, omdat dit kan leiden tot ontleding van het watervrije bariumchloride.
Het is belangrijk op te merken:
*Het exacte temperatuurbereik voor uitdroging kan enigszins variëren, afhankelijk van de specifieke omstandigheden.
* Dit proces moet worden uitgevoerd onder gecontroleerde omstandigheden en met gebruikmaking van de juiste veiligheidsmaatregelen, aangezien bariumchloride giftig kan zijn.
Als u voor een specifieke toepassing een precieze temperatuur nodig heeft, kunt u het beste een scheikundehandboek of wetenschappelijke literatuur raadplegen voor meer gedetailleerde informatie.
 Hoeveel representatieve deeltjes zijn er in 1,45 g van een moleculaire verbinding met molaire massa 237 g?
Hoeveel representatieve deeltjes zijn er in 1,45 g van een moleculaire verbinding met molaire massa 237 g?  Is de lipide dubbellaag het doorlatende voor de meeste in water oplosbare stoffen?
Is de lipide dubbellaag het doorlatende voor de meeste in water oplosbare stoffen?  Waar komen alle chemische reacties voor in een cel?
Waar komen alle chemische reacties voor in een cel?  Wat is het negatieve ion voor bariumsulfaat?
Wat is het negatieve ion voor bariumsulfaat?  Waterstof- en zuurstofdiffusie:gasbeweging begrijpen
Waterstof- en zuurstofdiffusie:gasbeweging begrijpen
 Daling van begrazingspraktijken bedreigt het bestaan van een Baskische kaas
Daling van begrazingspraktijken bedreigt het bestaan van een Baskische kaas Death metal - hoe nikkel een rol speelde bij 's werelds ergste massa-extinctie
Death metal - hoe nikkel een rol speelde bij 's werelds ergste massa-extinctie Uw favoriete visstroom loopt mogelijk een groot risico door de klimaatverandering. Hier leest u hoe u dat kunt weten
Uw favoriete visstroom loopt mogelijk een groot risico door de klimaatverandering. Hier leest u hoe u dat kunt weten  Onderzoek wijst uit dat de impact van tornadoschade tegen het einde van de 21e eeuw zou kunnen verdrievoudigen
Onderzoek wijst uit dat de impact van tornadoschade tegen het einde van de 21e eeuw zou kunnen verdrievoudigen Waarom het verbieden van financiering voor fossiele brandstofprojecten in Afrika geen klimaatoplossing is?
Waarom het verbieden van financiering voor fossiele brandstofprojecten in Afrika geen klimaatoplossing is?
Hoofdlijnen
- Doorbraak in genetisch onderzoek om gerstproductie te stimuleren
- Gevolgen van de microscoop op Science
- Wat gebeurt er nadat u een wortel in zout water hebt gestopt?
- Wat is een wetenschapsdefinitie voor mond?
- Uit onderzoek blijkt dat ongewervelde dieren een cruciale rol spelen als eco-beheerders in de mondiale afbraak van bosafval
- Wat betekent evolutie?
- Waarom is het nodig voor de cel om sommige cellulaire eiwitten af te breken?
- Welke insecten zijn de beste bestuivers?
- Is een ei biotisch of abiotisch?
- Hoog rijden? Chemici zetten stappen richting marihuana-ademanalysator

- Wat zit er in een permanente marker? Inkt, oplosmiddel en hars begrijpen

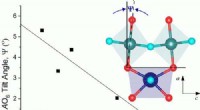
- Kennis opbouwen van veranderingen in de uraniumchemie
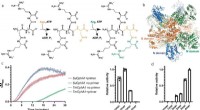
- De verrassende Zwitserse legermes-achtige functies van een krachtig enzym
- Hoe u nauwkeurig de pH van een mengsel van twee chemicaliën kunt berekenen

 Welk systeem bereidt voedsel voor op cellulair gebruik?
Welk systeem bereidt voedsel voor op cellulair gebruik?  Wat gebeurt er met klinkende golven als ze een muur of ander vast plat object bereiken?
Wat gebeurt er met klinkende golven als ze een muur of ander vast plat object bereiken?  Studie gebruikt AI-technologie om locaties van naschokken te voorspellen
Studie gebruikt AI-technologie om locaties van naschokken te voorspellen Hoe lang duurt het voordat de maan helemaal rond de aarde reizen?
Hoe lang duurt het voordat de maan helemaal rond de aarde reizen?  Een school met nieuwe gegevens over hoe het klimaat de visserij beïnvloedt
Een school met nieuwe gegevens over hoe het klimaat de visserij beïnvloedt  Is een gloeilamp een energiebron?
Is een gloeilamp een energiebron?  Hoe verwijder je chemische gifstoffen om het bloed en de urine gezond schoon te houden?
Hoe verwijder je chemische gifstoffen om het bloed en de urine gezond schoon te houden?  Kepler-telescoop ziet populatie vrij zwevende planeten
Kepler-telescoop ziet populatie vrij zwevende planeten
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

