
Wetenschap
Covalente bindingen en wateroplosbaarheid:de relatie begrijpen
Covalente bindingen zelf bepalen niet de oplosbaarheid in water. Het is het *molecuul* gevormd door die covalente bindingen dat er toe doet.
Dit is waarom:
* Water is een polair molecuul: Watermoleculen hebben een positief uiteinde (bij de waterstofatomen) en een negatief uiteinde (bij het zuurstofatoom). Door deze polariteit kan water sterke waterstofbruggen vormen met andere polaire moleculen.
* Polaire moleculen lossen op in water: Wanneer een polair molecuul zoals suiker (glucose) in water wordt gedaan, omringen de watermoleculen het suikermolecuul en vormen waterstofbruggen met de polaire groepen op de suiker. Deze interactie breekt het suikermolecuul uit elkaar en zorgt ervoor dat het oplost.
* Niet-polaire moleculen zijn onoplosbaar in water: Niet-polaire moleculen, zoals olie, hebben niet dezelfde polariteit. Watermoleculen kunnen er geen sterke waterstofbruggen mee vormen, dus blijven ze gescheiden en lossen ze niet op.
De oplosbaarheid van een covalente verbinding in water hangt dus af van de algehele polariteit:
* Polaire covalente moleculen: Deze moleculen hebben een ongelijkmatige verdeling van elektronen, waardoor gedeeltelijke ladingen ontstaan. Ze zijn *oplosbaar* in water omdat ze waterstofbruggen kunnen vormen met watermoleculen. Voorbeelden:suiker, ethanol.
* Niet-polaire covalente moleculen: Deze moleculen hebben een gelijkmatige verdeling van elektronen, waardoor er geen gedeeltelijke lading ontstaat. Ze zijn *onoplosbaar* in water omdat ze geen waterstofbruggen kunnen vormen met watermoleculen. Voorbeelden:olie, methaan.
Belangrijkste afhaalpunten: Het is niet de covalente binding zelf, maar de *polariteit* van het molecuul dat door de binding wordt gecreëerd, die de oplosbaarheid in water dicteert.
 Efficiënte katalysator op basis van titanium gebruikt om PEF te produceren, biobased alternatief voor PET
Efficiënte katalysator op basis van titanium gebruikt om PEF te produceren, biobased alternatief voor PET Nieuw katalysatorcomposiet vermindert het gebruik van zeldzame aardelementen
Nieuw katalysatorcomposiet vermindert het gebruik van zeldzame aardelementen Wat veroorzaakt die piek? Beantwoording van een al lang bestaande vraag over covalente vloeistoffen
Wat veroorzaakt die piek? Beantwoording van een al lang bestaande vraag over covalente vloeistoffen  Hoe afrodisiaca werken
Hoe afrodisiaca werken  Wat is het percentage samenstelling van zwavel in SO2?
Wat is het percentage samenstelling van zwavel in SO2?
 Hoe gletsjers aan het einde van de laatste ijstijd uit Schotland verdwenen
Hoe gletsjers aan het einde van de laatste ijstijd uit Schotland verdwenen Verschil tussen natuurlijke selectie en afstamming met wijziging
Verschil tussen natuurlijke selectie en afstamming met wijziging  Muizen krimpen, maar klimaatverandering en steden de schuld?
Muizen krimpen, maar klimaatverandering en steden de schuld?  Budgetvriendelijke manieren om aan uw vegetarische oplossing te komen als de prijzen stijgen
Budgetvriendelijke manieren om aan uw vegetarische oplossing te komen als de prijzen stijgen Het tappen van zoet water onder de oceaan heeft gevolgen
Het tappen van zoet water onder de oceaan heeft gevolgen
Hoofdlijnen
- Welk bestanddeel hebben alle basen gemeen?
- Wat is er in wat een lange streng DNA te vinden?
- Waarom is glyceraldehyde-3-fosfaat een belangrijk tussenliggend molecuul in de metabole routes omdat?
- Slechte zaden:hoe de ouderlijke afstamming de levensvatbaarheid van tomatenhybriden kan bepalen
- Relatie tussen DNA en natuurlijke selectie
- Welke soorten bewijs gebruiken wetenschappers om een organisme op een fylogene boom te plaatsen en wat vertelt die plaats je?
- Wat creëert eiwitten die door de cel worden gebruikt?
- Welk deel van een rode bloedcel geeft het de kleur en transporteert zuurstof?
- Twee organismen in dezelfde klasse maar verschillende orders zullen?
- Computermodel voor het ontwerpen van eiwitsequenties die zijn geoptimaliseerd om te binden aan medicijndoelen

- De beweging van fluorescerende sondes door het celmembraan stimuleren
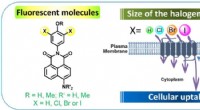
- Kettinglengte bepaalt moleculaire kleur, kleurafstemming voor medische beeldvorming mogelijk maken

- Potentieel nieuw zonnescherm is koraalveilig en biedt meer UVB/UVA-bescherming

- Milieuvriendelijke productie van geneesmiddelen Nobelprijswinnaars meest trotse prestatie

 De waarschuwende staart van komeet Swift-Tuttle
De waarschuwende staart van komeet Swift-Tuttle De energiebron die verantwoordelijk is voor de beweging van moleculen waaruit de atmosfeer bestaat, is een druk veroorzaakt door gewichtslucht B Zonage Power C Atmosferische getijden D Natuurlijke kinetische energie?
De energiebron die verantwoordelijk is voor de beweging van moleculen waaruit de atmosfeer bestaat, is een druk veroorzaakt door gewichtslucht B Zonage Power C Atmosferische getijden D Natuurlijke kinetische energie?  Top 6 bestemmingen in Texas voor het spotten van alligators
Top 6 bestemmingen in Texas voor het spotten van alligators  Welke golflengtamplitude?
Welke golflengtamplitude?  Is kracht gebaseerd op zowel massa als versnelling?
Is kracht gebaseerd op zowel massa als versnelling?  Houstons post-Harvey giftige puinhoop
Houstons post-Harvey giftige puinhoop Nieuwe look nodig? Online Makeover is fan-taaz-tisch
Nieuwe look nodig? Online Makeover is fan-taaz-tisch  Welk type kracht oefent u uit als uw stompvoet op de grond is?
Welk type kracht oefent u uit als uw stompvoet op de grond is?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

