
Wetenschap
Broom- en waterstofreactie:chemische vergelijking en uitleg
Hier is de uitgebalanceerde chemische vergelijking:
H₂ (g) + Br₂ (g) → 2HBr (g)
Belangrijkste punten:
* Voorwaarden: De reactie vereist warmte of licht om te starten. Dit komt omdat broom een diatomisch molecuul (Br₂) is en het verbreken van de binding energie kost.
* Mechanisme: De reactie verloopt via een radicaalmechanisme, waarbij broomradicalen (Br·) worden gevormd.
* Omkeerbaarheid: De reactie is omkeerbaar, wat betekent dat waterstofbromide onder bepaalde omstandigheden weer kan ontleden in waterstof en broom.
* Reactiepercentage: De snelheid van de reactie wordt beïnvloed door factoren zoals temperatuur, concentratie van reactanten en de aanwezigheid van katalysatoren.
* Veiligheid: Zowel waterstof als broom zijn gevaarlijke stoffen. De reactie moet worden uitgevoerd onder gecontroleerde omstandigheden met passende veiligheidsmaatregelen.
Gebruik van waterstofbromide:
* Industriële synthese: Waterstofbromide is een belangrijke industriële chemische stof die wordt gebruikt bij de productie van verschillende organische en anorganische verbindingen.
* Organische chemie: Het wordt gebruikt als katalysator en reagens bij verschillende organische reacties, waaronder alkylering en bromering.
* Farmaceutische producten: Het wordt gebruikt bij de synthese van sommige farmaceutische producten.
* Analytische chemie: Waterstofbromide wordt gebruikt als reagens in de analytische chemie, vooral bij de bepaling van bepaalde elementen.
 Dodelijke instorting van de dam in Brazilië roept angst op voor milieuproblemen
Dodelijke instorting van de dam in Brazilië roept angst op voor milieuproblemen Wat zijn de tien kenmerken van levende organismen?
Wat zijn de tien kenmerken van levende organismen?  Verband gevonden tussen Arctic Oscillation en verhoogd brandrisico in Siberië
Verband gevonden tussen Arctic Oscillation en verhoogd brandrisico in Siberië De implicaties bespreken voor een soort zelfbestuiving?
De implicaties bespreken voor een soort zelfbestuiving?  Wat is het klimaat en beschikt over extreme temperaturen en grasrijke vlakten die worden genoemd?
Wat is het klimaat en beschikt over extreme temperaturen en grasrijke vlakten die worden genoemd?
Hoofdlijnen
- Waarom is het gunstig voor organismen om seksueel en aseksueel te produceren?
- Hoe functioneren cellen als de kleinste levenseenheid?
- Wat is de beweging van chemische stoffen die meestal over het celmembraan opnieuw een concentratiegradiënt vereist, vereist cellen naar energie?
- Waar is een pasgeboren baby -skelet van gemaakt?
- Wat is het verschil tussen biotische en abiotische factoren geven een voorbeeld van elk?
- Wat is biologische besmetting die voortvloeit uit weersomstandigheden?
- Alle cellen converteren de potentiële energie die wordt gevonden in voedsemoleculen in ATP door?
- Nieuwe functie in genregulerend eiwit ontdekt
- Fosfofructokinase (PFK):allosterische regulatie begrijpen
- Op palladium gebaseerd metaalglas met hoge trombogene weerstand
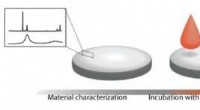
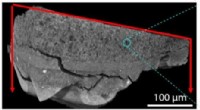
- Wetenschappers onderzoeken verouderde verf in microscopisch detail om de conserveringsinspanningen te informeren
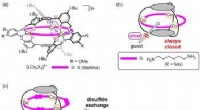
- Een gesloten kooi-achtig molecuul dat kan worden geopend
- Maakt het mogelijk om grotere 3D-geprinte objecten te maken met keramiek

- PEF daagt PET uit voor de strijd

 Differentiëren tussen energie verkregen door het verbranden van fossiele brandstoffen en dat als zonne -energie?
Differentiëren tussen energie verkregen door het verbranden van fossiele brandstoffen en dat als zonne -energie?  Waarom de Quagga, een ondersoort van de zebra, uitstierf
Waarom de Quagga, een ondersoort van de zebra, uitstierf  Welke term verwijst naar al het landoppervlak van de aarde?
Welke term verwijst naar al het landoppervlak van de aarde?  Thermisch geactiveerde vertraagde fotoluminescentie van halfgeleider nanokristallen
Thermisch geactiveerde vertraagde fotoluminescentie van halfgeleider nanokristallen De lessen delen die zijn geleerd tijdens de overstroming van Colorado in 2013
De lessen delen die zijn geleerd tijdens de overstroming van Colorado in 2013 In de Gravitational Force -formule als je een van de massa's verdubbelt en drievoudige tweede nieuw wordt?
In de Gravitational Force -formule als je een van de massa's verdubbelt en drievoudige tweede nieuw wordt?  Wat betekent conclusie en discussie in een wetenschap?
Wat betekent conclusie en discussie in een wetenschap?  Transparant kunstparelmoer:een bakstenen muur op nanoschaal
Transparant kunstparelmoer:een bakstenen muur op nanoschaal
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

