
Wetenschap
Elektrische geleidbaarheid van materialen:obligaties en vaste toestand
Materialen die elektriciteit in de vaste toestand geleiden:
* Metaalverbindingen: Deze worden gevormd door een "zee" van gedelokaliseerde elektronen die vrij zijn om door de structuur van het metaal te bewegen. Deze vrije beweging van elektronen zorgt voor een uitstekende elektrische geleiding. Voorbeelden:koper, goud, zilver, aluminium.
* Sommige covalente verbindingen: Hoewel bij covalente bindingen doorgaans gedeelde elektronen betrokken zijn, hebben bepaalde covalente verbindingen elektronen die relatief losjes vastgehouden worden en binnen de kristalstructuur kunnen bewegen. Deze materialen worden halfgeleiders genoemd en hun geleidbaarheid kan worden beïnvloed door temperatuur of onzuiverheden. Voorbeelden:silicium, germanium.
Materialen die alleen elektriciteit geleiden als ze gesmolten of opgelost zijn in water:
* Ionische verbindingen: Ionische bindingen worden gevormd door de elektrostatische aantrekkingskracht tussen positief en negatief geladen ionen. In de vaste toestand worden deze ionen vastgehouden in een stijf rooster en kunnen ze niet vrij bewegen. Wanneer ze echter worden gesmolten of opgelost in water, worden de ionen mobiel en kunnen ze elektrische stroom transporteren. Voorbeelden:Natriumchloride (NaCl), kaliumbromide (KBr).
Belangrijkste punten:
* Vrije elektronenbeweging: Elektrische geleidbaarheid is fundamenteel afhankelijk van het vermogen van geladen deeltjes (elektronen of ionen) om vrij te bewegen.
* Hechting en geleidbaarheid: Het type chemische binding bepaalt de mobiliteit van deze geladen deeltjes.
* Halfgeleiders: Deze materialen fungeren als een brug tussen geleiders en isolatoren. Hun geleidbaarheid kan worden gecontroleerd door externe factoren.
Laat het me weten als je nog vragen hebt over geleidbaarheid of bonding!
 Hoeveel atomen zijn er in 0,5 mol AR?
Hoeveel atomen zijn er in 0,5 mol AR?  Onder anaërobe omstandigheden kunnen gewone microbiële gemeenschappen de ultrasterke koolstof-fluorbinding verbreken
Onder anaërobe omstandigheden kunnen gewone microbiële gemeenschappen de ultrasterke koolstof-fluorbinding verbreken Wat is lipide polymeer?
Wat is lipide polymeer?  Hoe u de calorimeterconstante kunt berekenen:een stapsgewijze handleiding
Hoe u de calorimeterconstante kunt berekenen:een stapsgewijze handleiding  Hoe maak je onderscheid tussen de gassen H2 en NO2?
Hoe maak je onderscheid tussen de gassen H2 en NO2?
 Wetlands, onze levensondersteunende systemen, meer nodig hebben dan druppel-voor-druppel-hulp, waarschuwt nieuw rapport
Wetlands, onze levensondersteunende systemen, meer nodig hebben dan druppel-voor-druppel-hulp, waarschuwt nieuw rapport Zout in zeespray blijkt de reden te zijn voor minder bliksem boven tropische oceanen
Zout in zeespray blijkt de reden te zijn voor minder bliksem boven tropische oceanen Rivieren veranderen voortdurend, en het beïnvloedt hun vermogen om overstromingen in te dammen
Rivieren veranderen voortdurend, en het beïnvloedt hun vermogen om overstromingen in te dammen Wetenschappers publiceren allereerste rapport over landgezondheid
Wetenschappers publiceren allereerste rapport over landgezondheid Aanwijzingen over hoe bodems kunnen reageren op klimaatverandering gevonden
Aanwijzingen over hoe bodems kunnen reageren op klimaatverandering gevonden
Hoofdlijnen
- Welk type decolleté vormt zich bij de beginnende celdeling?
- Wat is de ideale osmotische omgeving voor een dierencel?
- Hoe noem je een embryo tijdens de late stadia van ontwikkeling?
- Wat zijn de vier basistypen weefsels in planten?
- Is er een relatie tussen voedsel en uw bloedtype?
- Zijn antigeen in combinatie met oligosachariden?
- Hoe verschilt celdeling bij dieren van planten?
- Meer natuurlijk voorkomende bomen en minder clustering kunnen stedelijke bossen ten goede komen
- Wat is het verschil tussen allelen en genen?
- Een nanostructuur van silica met chemo-enzymatische compartimentering

- Neutronendiffractie-experimenten van materialen met structuren die meerdere metalen elementen bevatten

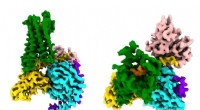
- CryoEM-onderzoek legt opioïde-signalering vast
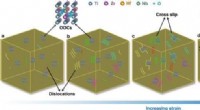
- Verbeterde sterkte en taaiheid in een legering met hoge entropie via geordende zuurstofcomplexen
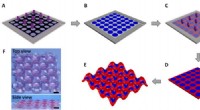
- Hydrogels met periodiek patroon:een model voor coöperatieve vervorming
 Wat stelt cellen in staat om energie om te zetten in afwezigheid van zuurstof?
Wat stelt cellen in staat om energie om te zetten in afwezigheid van zuurstof?  Welk pad illustreert het beste een manier om te reist door een bosecosysteem dat bestaat uit muizenuilplantslang en zon?
Welk pad illustreert het beste een manier om te reist door een bosecosysteem dat bestaat uit muizenuilplantslang en zon?  Is silicium het op een na meest voorkomende element in de biosfeer?
Is silicium het op een na meest voorkomende element in de biosfeer?  Wat is de enige cel in het menselijk lichaam met een kern?
Wat is de enige cel in het menselijk lichaam met een kern?  Onafhankelijk, particuliere bedrijven vervuilen minder dan overheidsbedrijven, studie toont
Onafhankelijk, particuliere bedrijven vervuilen minder dan overheidsbedrijven, studie toont Natuurkundigen beslechten controverse over identieke deeltjesverstrengeling
Natuurkundigen beslechten controverse over identieke deeltjesverstrengeling Wat is de willekeurige moleculaire van een substantie grootst wanneer is?
Wat is de willekeurige moleculaire van een substantie grootst wanneer is?  Is tafelzout een stof of mengsel?
Is tafelzout een stof of mengsel?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

