
Wetenschap
Lewis-structuur van N2H2Cl2:stapsgewijze handleiding en uitleg
1. Valentie-elektronen tellen:
* Stikstof (N) heeft elk 5 valentie-elektronen (2 N-atomen =10 elektronen)
* Waterstof (H) heeft elk 1 valentie-elektron (2 H-atomen =2 elektronen)
* Chloor (Cl) heeft elk 7 valentie-elektronen (2 Cl-atomen =14 elektronen)
* Totale valentie-elektronen =10 + 2 + 14 =26 elektronen
2. Centraal Atoom:
* Stikstof is het minst elektronegatieve element en zal dus het centrale atoom zijn.
3. Enkelvoudige obligaties:
* Verbind de atomen met enkele bindingen.
* Hierbij worden 6 elektronen gebruikt (3 bindingen x 2 elektronen/binding).
4. Resterende elektronen:
*Je hebt nog 20 elektronen over (26 - 6).
5. Octet vullen voor buitenste atomen:
* Vul de octetten (8 elektronen) voor de waterstof- en chlooratomen aan door alleenstaande paren toe te voegen.
*Hierbij worden 12 elektronen gebruikt (2 H-atomen x 2 elektronen + 2 Cl-atomen x 3 elektronen).
6. Octet voor centrale atomen vullen:
*De stikstofatomen hebben nu elk 6 elektronen. Geef elk stikstofatoom één eenzaam paar. Hierbij worden de resterende 8 elektronen gebruikt.
7. Controleer op formele aanklacht:
* Bereken de formele lading van elk atoom om er zeker van te zijn dat de structuur het meest stabiel is. De formele lading moet zo dicht mogelijk bij nul liggen.
* Formele lading =(Valentie-elektronen) - (Niet-bindende elektronen) - (1/2 bindende elektronen)
Lewis-structuur:
```
H Cl
\ /
N-N
/ \
Cl H
```
Belangrijke opmerkingen:
* Dit molecuul heeft resonantiestructuren, wat betekent dat de dubbele binding tussen de twee stikstofatomen kan verschuiven.
* Het molecuul heeft een vlakke geometrie.
* De N-Cl-bindingen zijn polair en het molecuul als geheel is ook polair.
 Wat rechtvaardigde Charles Origin of Soorten?
Wat rechtvaardigde Charles Origin of Soorten?  Studiegegevens begeleiden belangrijke beleidsbeslissingen op het gebied van transport en landgebruik
Studiegegevens begeleiden belangrijke beleidsbeslissingen op het gebied van transport en landgebruik Studies tonen aan dat wereldwijde schattingen van het smelten van ijs conservatief zijn geweest
Studies tonen aan dat wereldwijde schattingen van het smelten van ijs conservatief zijn geweest Hoe een onbekend genotype te bepalen met behulp van een test Cross
Hoe een onbekend genotype te bepalen met behulp van een test Cross Eindeloze winter:de storm die het surfen in Californië definieerde
Eindeloze winter:de storm die het surfen in Californië definieerde
Hoofdlijnen
- Law of Segregation (Mendel): definitie, toelichting en voorbeelden
- Wat zijn de verschillen in sets van allelen tussen individuen die een populatie heeft genoemd?
- Waarom kunnen dieren- en plantencellen niet worden geclassificeerd als prokaryote?
- Hoe biologische landbouw werkt
- Wat voor soort planten leven in zout water waren zeesterren leven?
- Roundworms hebben spierweefsel en een darm met één opening?
- Welke soorten organismen hebben gespecialiseerde cellen?
- Onderzoek onthult hoe cellen zich herbouwen na mitose
- Wat is de verdediging van heterozygote en homozygoot?
- Het bouwen van een betere brandstofcel begint met oppervlaktechemie

- Een doorbraak in katalysatoren:kleiner dan nanoschaal

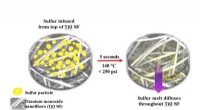
- Een stabiliserende invloed maakt de evolutie van lithium-zwavelbatterijen mogelijk
- Vloeistof heeft structuur, wat de sleutel kan zijn tot het begrijpen van metaalglas

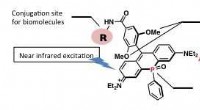
- Een nabij-infrarood fluorescerende kleurstof voor bio-imaging op lange termijn
 Is parasitisme een vorm van symbiose?
Is parasitisme een vorm van symbiose?  Resonantie Raman-verstrooiing biedt nieuwe manieren voor zeer gevoelige temperatuurmeting
Resonantie Raman-verstrooiing biedt nieuwe manieren voor zeer gevoelige temperatuurmeting Waarom bestuderen wetenschappers menselijk DNA?
Waarom bestuderen wetenschappers menselijk DNA?  Planten met inkteigenschappen
Planten met inkteigenschappen  Ontwerpen van een atomaire opstelling met meerdere elementen
Ontwerpen van een atomaire opstelling met meerdere elementen Een makkelijke pil om te slikken:nieuw onderzoek naar 3D-printen maakt de weg vrij voor gepersonaliseerde medicatie
Een makkelijke pil om te slikken:nieuw onderzoek naar 3D-printen maakt de weg vrij voor gepersonaliseerde medicatie  Welke plaats ligt 30 graden noord en 75 oost?
Welke plaats ligt 30 graden noord en 75 oost?  Welke afstand resulteert in de sterkste magnetische aantrekkingskracht?
Welke afstand resulteert in de sterkste magnetische aantrekkingskracht?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

