
Wetenschap
Intermoleculaire krachten:F2 versus Cl2 - Welke is sterker?
Dit is waarom:
* Londense verspreidingstroepen: Zowel F₂ als Cl₂ zijn niet-polaire moleculen, dus de enige intermoleculaire krachten die ze ervaren zijn Londense dispersiekrachten. Deze krachten komen voort uit tijdelijke fluctuaties in de elektronenverdeling binnen het molecuul, waardoor tijdelijke dipolen ontstaan.
* Grootte en polariseerbaarheid: Chlooratomen zijn groter dan fluoratomen. Grotere atomen hebben meer elektronen, en deze elektronen bevinden zich verder van de kern. Dit maakt ze polariseerbaarder, wat betekent dat hun elektronenwolken gemakkelijker kunnen worden vervormd om tijdelijke dipolen te creëren.
* Kracht van de Londense verspreidingskrachten: Grotere, meer polariseerbare moleculen hebben sterkere Londense dispersiekrachten. Omdat Cl₂ groter en polariseerbaarder is dan F₂, zijn de Londense dispersiekrachten sterker.
Samengevat: De sterkere Londense dispersiekrachten in Cl₂, vanwege de grotere omvang en grotere polariseerbaarheid, zorgen ervoor dat het sterkere intermoleculaire krachten heeft dan F₂.
 Nieuwe benadering van prognoses van de opwarming van de aarde kan regionale schattingen nauwkeuriger maken
Nieuwe benadering van prognoses van de opwarming van de aarde kan regionale schattingen nauwkeuriger maken Hoe we een Arctisch kwikmysterie hebben opgelost
Hoe we een Arctisch kwikmysterie hebben opgelost Afrikaans rookwolkverbindingsdoel van NASA-vluchten in de lucht
Afrikaans rookwolkverbindingsdoel van NASA-vluchten in de lucht Maanden nodig voor aanvullende studie van Dakota Access-pijplijn
Maanden nodig voor aanvullende studie van Dakota Access-pijplijn Nieuwe nachtverlichtingskaarten openen mogelijke realtime toepassingen
Nieuwe nachtverlichtingskaarten openen mogelijke realtime toepassingen
Hoofdlijnen
- Het belangrijkste orgaan in ons lichaam zijn de hersenen?
- Overlevingsstrategie:hoe één enzym bacteriën helpt herstellen van blootstelling aan antibiotica
- Wat is de ORF van een gen?
- Wat doet de kern in het lichaam?
- Waarom denk je dat er weinig bekend was over cellen vóór de uitvinding van de microscoop?
- Eerste Amerikaanse vrouw bevalt van getransplanteerde baarmoeder
- Beschrijf soorten hersenen met diagram?
- Identificeer twee factoren die enzym denaturatie kunnen veroorzaken?
- 3 weefsels die het vasculaire systeem vormen in een zaadplant?
- De vijf essentiële eigenschappen van water die het leven in stand houden

- Nieuwe methodologie helpt bij het bestuderen van veelbelovende gerichte steigers voor medicijnafgifte

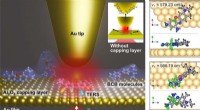
- Voor het eerst het verschil in structurele dynamiek van 1 nm enkelvoudige moleculen bij kamertemperatuur waarnemen
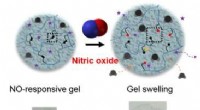
- Wetenschappers ontwikkelen potentieel therapeutische gel, die stikstofmonoxide detecteert, absorbeert overtollig vocht en geeft medicijnen af
- Flexibele elektronische huid helpt mens-machine-interacties

 Hoe roltrappen werken:een technisch overzicht
Hoe roltrappen werken:een technisch overzicht  Wat is de kracht die een object in tegengestelde richting van objectenbeweging duwt?
Wat is de kracht die een object in tegengestelde richting van objectenbeweging duwt?  Wat zijn de drie horizonten van een volwassen restbodem?
Wat zijn de drie horizonten van een volwassen restbodem?  Een mensachtige planner waarmee robots objecten in een rommelige omgeving kunnen bereiken
Een mensachtige planner waarmee robots objecten in een rommelige omgeving kunnen bereiken Zou jij je kinderen laten vervoeren door een dienst? Sommige ouders doen dat al
Zou jij je kinderen laten vervoeren door een dienst? Sommige ouders doen dat al  Waterige oplossingen van bariumnitraat en natriumhydroxide worden gecombineerd, vormt zich een neerslag?
Waterige oplossingen van bariumnitraat en natriumhydroxide worden gecombineerd, vormt zich een neerslag?  Wanneer moleculen botsen en energie overdragen, wordt het hoe heet hoe?
Wanneer moleculen botsen en energie overdragen, wordt het hoe heet hoe?  Als je een bal omhoog gooit, wat gebeurt er met zijn snelheid, terwijl het omhoog gaat?
Als je een bal omhoog gooit, wat gebeurt er met zijn snelheid, terwijl het omhoog gaat?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

