
Wetenschap
Behoud van het massagetal in chemische vergelijkingen:een uitgebreide gids
Het totale massagetal van de reactanten is gelijk aan het totale massagetal van de producten.
Hier is hoe het werkt:
* Massagetal: Het massagetal van een atoom is de som van zijn protonen en neutronen.
* Chemische reacties: Bij chemische reacties worden atomen herschikt, niet gecreëerd of vernietigd. Het aantal protonen en neutronen in elk atoom blijft hetzelfde.
* Behoud: Dit betekent dat het totale aantal protonen en neutronen aan de reactantzijde van de vergelijking gelijk moet zijn aan het totale aantal aan de productzijde.
Voorbeeld:
Denk aan de verbranding van methaan (CH₄):
CH₄ + 2O₂ → CO₂ + 2H₂O
* Reactanten:
* CH₄:Massagetal =12 (C) + 4 (H) =16
* 2O₂:Massagetal =2 * 32 (O) =64
* Totaal massanummer van de reactant =16 + 64 =80
* Producten:
* CO₂:Massagetal =12 (C) + 2 * 16 (O) =44
* 2H₂O:Massagetal =2 * (2 (H) + 16 (O)) =36
* Totaal productmassanummer =44 + 36 =80
Het totale massagetal aan de reactantzijde (80) is gelijk aan het totale massagetal aan de productzijde (80). Daarom wordt in deze chemische vergelijking voldaan aan het principe van behoud van het massagetal.
Belangrijkste punten:
* Het principe van behoud van massagetal wordt ook wel behoud van nucleonen genoemd .
* Het is belangrijk om te onthouden dat dit principe van toepassing is op kernreacties ook waar het aantal protonen en neutronen kan veranderen.
* Het balanceren van chemische vergelijkingen zorgt voor het behoud van het massagetal.
Laat het me weten als je nog vragen hebt!
 Las Vegas weegt het koppelen van groei aan natuurbehoud te midden van droogte
Las Vegas weegt het koppelen van groei aan natuurbehoud te midden van droogte Welk proces verwering of erosie is gemakkelijker te zien daadwerkelijk plaatsvinden?
Welk proces verwering of erosie is gemakkelijker te zien daadwerkelijk plaatsvinden?  Gefossiliseerde boom en ijskernen helpen bij het dateren van enorme vulkaanuitbarsting 1, 000 jaar geleden tot binnen drie maanden
Gefossiliseerde boom en ijskernen helpen bij het dateren van enorme vulkaanuitbarsting 1, 000 jaar geleden tot binnen drie maanden Leiden massaschietpartijen tot meer schietpartijen? Onderzoek is verdeeld
Leiden massaschietpartijen tot meer schietpartijen? Onderzoek is verdeeld  Bepalen welke soorten bossen de meeste koolstof kunnen opslaan en onder welke omstandigheden
Bepalen welke soorten bossen de meeste koolstof kunnen opslaan en onder welke omstandigheden
Hoofdlijnen
- Welke organel draagt stoffen naar andere delen van een cel?
- Noem twee dingen die worden gevonden in een plantencel die geen dierencel zijn-?
- Deze spitsmuizen hebben koppen die krimpen met het seizoen
- Welk idee heeft L Lynn Margulis voorgesteld om de oorsprong van organellen uit te leggen?
- Welke organismen die kunnen paren en vruchtbare nakomelingen produceren?
- Wat is een duidelijk membraan?
- De naam gegeven aan een organisme dat de minste verwarring veroorzaakt en hetzelfde is in een taal of land de?
- Welk kenmerk gebruikelijk voor alle schimmels?
- Waarom algemene namen voor organismen problematisch zijn:dubbelzinnigheid en onnauwkeurigheid
- Wetenschappers ontwikkelen nieuwe technologie voor de winning van non-ferro en edelmetalen

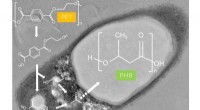
- Hoe een bacterie de plasticvervuilingscrisis kan helpen oplossen
- Poreuze polymeercoatings regelen dynamisch licht en warmte

- Kunstmatige intelligentie versnelt fotodynamische simulaties

- Waarom scheren zelfs de scherpste scheermessen dof maakt

 Nieuwe studie toont aan dat opslag van koolstofdioxide een veilig hulpmiddel is om klimaat te verminderen
Nieuwe studie toont aan dat opslag van koolstofdioxide een veilig hulpmiddel is om klimaat te verminderen Gebruikmakend van de eigenschappen van een opmerkelijk 2D-materiaal
Gebruikmakend van de eigenschappen van een opmerkelijk 2D-materiaal Waarom wordt MnO2 toegevoegd aan de ontleding van de H2O2-reactie?
Waarom wordt MnO2 toegevoegd aan de ontleding van de H2O2-reactie?  Hoe de schedel van de oudst bekende voorouder van de mensheid ons begrip van de evolutie verandert
Hoe de schedel van de oudst bekende voorouder van de mensheid ons begrip van de evolutie verandert  Hoe een kernoorlog de aarde vandaag zou beïnvloeden
Hoe een kernoorlog de aarde vandaag zou beïnvloeden Welke technologie zou de meeste energie in lichtgolven produceren?
Welke technologie zou de meeste energie in lichtgolven produceren?  Waarom produceert de Hubble -telescoop in de ruimte betere afbeeldingen dan landgebaseerde telescopen?
Waarom produceert de Hubble -telescoop in de ruimte betere afbeeldingen dan landgebaseerde telescopen?  Het belangrijkste punt dat rekening houdt met de transmissie en verdeling van elektrische energie?
Het belangrijkste punt dat rekening houdt met de transmissie en verdeling van elektrische energie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

