
Wetenschap
Aluminiumchloride (AlCl3):covalent of ionisch karakter?
* Ionisch karakter: Aluminium (Al) is een metaal en chloor (Cl) is een niet-metaal. Metalen hebben de neiging elektronen te verliezen en positieve ionen (kationen) te vormen, terwijl niet-metalen de neiging hebben elektronen te winnen en negatieve ionen (anionen) te vormen. Dit verschil in elektronegativiteit leidt tot een ionische interactie.
* Covalent karakter: Het elektronegativiteitsverschil tussen aluminium en chloor is niet extreem groot. Dit leidt tot een aanzienlijke mate van covalent karakter in de obligaties. De elektronen worden niet volledig overgedragen van aluminium naar chloor, maar worden tot op zekere hoogte gedeeld.
Samengevat:
* AlCl3 vertoont kenmerken van zowel ionische als covalente binding.
* De binding in AlCl3 kan het beste worden omschreven als polair covalent .
* Het is belangrijk op te merken dat de binding in de meeste verbindingen ergens in het spectrum tussen puur ionisch en puur covalent valt.
 In een nucleaire fusiereactie is de massa producten?
In een nucleaire fusiereactie is de massa producten?  Wat zijn de eigenschappen van Gallium?
Wat zijn de eigenschappen van Gallium?  Magnesium plus zinksulfaat - magnesiumzink?
Magnesium plus zinksulfaat - magnesiumzink?  Wanneer 2 vloeistoffen worden gemengd en warmte wordt ontwikkeld Welk type oplossing is gevormd, wat is de afwijking?
Wanneer 2 vloeistoffen worden gemengd en warmte wordt ontwikkeld Welk type oplossing is gevormd, wat is de afwijking?  Als je je handen tegen elkaar wrijft, ontstaat er een beetje warmte. Beschrijf de energiestroom die ervoor zorgt dat warmte wordt geproduceerd. gebruik de term chemische kinetische wrijving en als antwoord?
Als je je handen tegen elkaar wrijft, ontstaat er een beetje warmte. Beschrijf de energiestroom die ervoor zorgt dat warmte wordt geproduceerd. gebruik de term chemische kinetische wrijving en als antwoord?
 Wijdverbreide ineenstorting van de ijskap van West-Antarctica is te vermijden als we de opwarming van de aarde onder de 2 graden houden
Wijdverbreide ineenstorting van de ijskap van West-Antarctica is te vermijden als we de opwarming van de aarde onder de 2 graden houden De mensheid moet oceanen redden om zichzelf te redden, VN waarschuwt
De mensheid moet oceanen redden om zichzelf te redden, VN waarschuwt Vulkaanmuziek kan wetenschappers helpen uitbarstingen te volgen
Vulkaanmuziek kan wetenschappers helpen uitbarstingen te volgen Historische deal herleeft plan voor grootste Amerikaanse damsloop
Historische deal herleeft plan voor grootste Amerikaanse damsloop KAN WETENSCHAPPER DEZELFDE PRINCIPES GEBRUIKEN OM DE GESCHIEDENIS VAN DE AARDE TE BESTUDEREN?
KAN WETENSCHAPPER DEZELFDE PRINCIPES GEBRUIKEN OM DE GESCHIEDENIS VAN DE AARDE TE BESTUDEREN?
Hoofdlijnen
- Genealogie:onderzoek naar uw familiegeschiedenis en afkomst
- Worden leiders geboren of gemaakt? Nieuw onderzoek laat zien hoe leiderschap zich ontwikkelt
- Wat zijn de structuren en functies van het perifere systeem van het centrale zenuwstelsel?
- Kan een criticus die een gelovige is geworden, anderen beïnvloeden? Het geval van genetisch gemodificeerd voedsel
- Heeft de eiercel veel cellen?
- Welk type weefsel bedekt het lichaamsoppervlak en lijnen organen?
- Welke observatie bewijst dat een cel eukatyotes is?
- Hoe cellen hun microtubuli-skelet samenstellen
- Hoe werken het ademhalings- en cardiovasculaire systeem samen?
- Hoe gemeenschappelijke elementen een meer energiezekere toekomst kunnen maken

- Nieuw begrip van de synthese van antibiotica
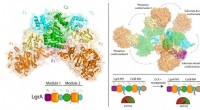
- Een weg om defecten tijdens additive manufacturing te vermijden

- Deze op RNA gebaseerde techniek zou gentherapie effectiever kunnen maken

- Nieuw multi-protondragercomplex als efficiënte protongeleider bij hoge temperaturen
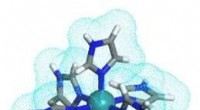
 Beschrijf hoe de weerstand van een materiaal wordt bepaald?
Beschrijf hoe de weerstand van een materiaal wordt bepaald?  12 oz gelijk aan 1 pond?
12 oz gelijk aan 1 pond?  Ik geef de voorkeur aan een enkellabel:waarom thuisquarantaine-apps een slecht idee zijn
Ik geef de voorkeur aan een enkellabel:waarom thuisquarantaine-apps een slecht idee zijn Vijf redenen waarom zwerfafval slecht is
Vijf redenen waarom zwerfafval slecht is De prestaties van halfgeleiders testen - met licht
De prestaties van halfgeleiders testen - met licht Welke planeet wanneer bekeken door een telescoop verschijnt als roodachtige bal onderbroken door enkele permanente donkere gebieden die intensiteit veranderen?
Welke planeet wanneer bekeken door een telescoop verschijnt als roodachtige bal onderbroken door enkele permanente donkere gebieden die intensiteit veranderen?  Hoe gebeurt de thermische geleiding het snelst?
Hoe gebeurt de thermische geleiding het snelst?  Eten of helpen zebramosselen giftige algen?
Eten of helpen zebramosselen giftige algen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

