
Wetenschap
Wat zijn de eigenschappen van Gallium?
eigenschappen van gallium:
Fysieke eigenschappen:
* uiterlijk: Zilverachtige, zachte en kneedbare vaste stof bij kamertemperatuur.
* smeltpunt: 29,76 ° C (85,57 ° F). Dit is net boven kamertemperatuur, waardoor het een van de weinige metalen is die vloeibaar zijn bij kamertemperatuur (de andere is kwik).
* kookpunt: 2204 ° C (3999 ° F).
* Dichtheid: 5,91 g/cm³ bij 25 ° C.
* elektrische geleidbaarheid: Goede geleider van elektriciteit.
* Thermische geleidbaarheid: Slechte dirigent van warmte.
* kristalstructuur: Orthorhombisch.
* isotopen: Natuurlijk voorkomend gallium heeft twee isotopen:⁶⁹GA (60,11%) en ⁷¹ga (39,89%).
chemische eigenschappen:
* Reactiviteit: Matig reactief metaal.
* Oxidatie stelt: +1, +2 en +3, waarbij +3 de meest voorkomende is.
* Chemische reacties: Reageert met zuren en alkalis om zouten te vormen.
* Vorming van verbindingen: Vormt verschillende verbindingen, waaronder galliumarsenide (GaAs) en galliumnitride (GAN), die belangrijke halfgeleiders zijn.
* Oplosbaarheid: Onoplosbaar in water maar oplosbaar in zuren.
Andere opmerkelijke eigenschappen:
* Unieke uitbreiding bij stolling: In tegenstelling tot de meeste materialen breidt Gallium uit bij stolling, vergelijkbaar met water. Dit maakt het geschikt voor gebruik in hoge druktoepassingen.
* Lage dampdruk: Heeft een zeer lage dampdruk, waardoor het geschikt is voor gebruik in omgevingen met een hoge vacuüm.
* Bevestigende eigenschap: Gallium kan nat glas en vele andere materialen, wat nuttig kan zijn in bepaalde toepassingen.
Gebruik van gallium:
* halfgeleiders: Gallium-arsenide (GaAs) en galliumnitride (GAN) worden gebruikt in snelle elektronica, lasers, zonnecellen en LED-verlichting.
* geneeskunde: Gallium-67 wordt in nucleaire geneeskunde gebruikt om tumoren en infecties te beelden.
* spiegels: Vloeibare gallium kan worden gebruikt om zeer reflecterende spiegels te maken.
* thermometers op hoge temperatuur: Vanwege het hoge kookpunt en lage dampdruk kan gallium worden gebruikt om thermometers op hoge temperatuur te creëren.
* Andere toepassingen: Gallium wordt ook gebruikt in legeringen, katalysatoren en als dopant in siliciumwafels.
Veiligheidsoverwegingen:
* toxiciteit: Gallium wordt beschouwd als lage toxiciteit, maar langdurige blootstelling kan leiden tot gezondheidsproblemen.
* contact met de huid: Vermijd contact met de huid omdat dit irritatie kan veroorzaken.
Samenvattend: Gallium is een fascinerend element met unieke eigenschappen die het op verschillende gebieden waardevol maken, met name in elektronica, geneeskunde en toepassingen op hoge temperatuur.
 Wat gebeurt er met de ozonlaag in Stratoshere?
Wat gebeurt er met de ozonlaag in Stratoshere?  Wat is een mengsel of metaalachtige vaste oplossing bestaande uit 2 elementen?
Wat is een mengsel of metaalachtige vaste oplossing bestaande uit 2 elementen?  Wat zal een afname van de gasdruk in een gesloten container veroorzaken?
Wat zal een afname van de gasdruk in een gesloten container veroorzaken?  Wat is het verschil tussen chemische versus fysische verandering?
Wat is het verschil tussen chemische versus fysische verandering?  Het nieuwe groene alternatief voor de productie van medicijnen
Het nieuwe groene alternatief voor de productie van medicijnen
 Optimisme wint van wanhoop op klimaattop
Optimisme wint van wanhoop op klimaattop Wat is de term die wordt gebruikt om een verklaring te beschrijven van een natuurlijk fenomeen dat wordt ondersteund door observatie en experimenten?
Wat is de term die wordt gebruikt om een verklaring te beschrijven van een natuurlijk fenomeen dat wordt ondersteund door observatie en experimenten?  Waarom is het belangrijk om de natuur te kennen?
Waarom is het belangrijk om de natuur te kennen?  De huidige toezeggingen om steenkoolstroom uit te faseren zijn kritisch onvoldoende om de klimaatverandering te vertragen
De huidige toezeggingen om steenkoolstroom uit te faseren zijn kritisch onvoldoende om de klimaatverandering te vertragen Wat is pad- of statushoeveelheid?
Wat is pad- of statushoeveelheid?
Hoofdlijnen
- Wat maakt evolutie een therory?
- Is RNA of DNA het belangrijkst voor het virus?
- Waarom is het een voordeel voor een schimmel om ondergronds fruitlichaam te ontwikkelen en alleen te zijn ontstaan als ze bijna volwassen zijn?
- Wat zijn de belangrijkste verschillen tussen plantaardige en dierlijke cellen?
- Vaccinia-virus:nieuwe inzichten in de structuur en functie van het pokkenvirus-prototype
- Wat zijn plantesimals?
- Hoe te metaboliseren glucose om ATP te maken
Energie opgeslagen in de chemische bindingen van de koolhydraat-, vet- en eiwitmoleculen in levensmiddelen. Het proces van spijsvertering breekt koolhydraatmoleculen af in glucosemoleculen. Glucose die
- Waar vindt aerobe en anerobe ademhaling plaats?
- Hoe genoctrooien werken
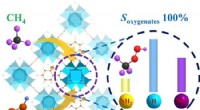
- Onderzoekers stellen nieuwe strategie voor om methaanhydroxylering te verbeteren
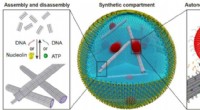
- Nog een stap in de richting van synthetische cellen
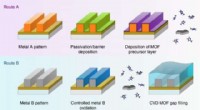
- Nieuwe isolatietechniek maakt de weg vrij voor krachtigere en kleinere spanen
- Materiaal voor veiligere voetbalhelmen kan hoofdletsel verminderen

- Een gemakkelijke weg naar polymeercoatings met potentieel gebruik bij het voorkomen van biofouling
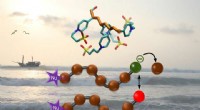
 Welke bindingen worden gevormd door de aantrekkingskracht van tegengesteld geladen ionen?
Welke bindingen worden gevormd door de aantrekkingskracht van tegengesteld geladen ionen?  Hoe tijd met uw schaduw te vertellen
Hoe tijd met uw schaduw te vertellen  Onderzoek naar nieuwe fysica die voortkomt uit elektroneninteracties in halfgeleider-moiré-superroosters
Onderzoek naar nieuwe fysica die voortkomt uit elektroneninteracties in halfgeleider-moiré-superroosters  Wat zijn procedures van een project voor zonnestelsels?
Wat zijn procedures van een project voor zonnestelsels?  Onderzoekers ontdekken hoe licht elektronen in metaal exciteert
Onderzoekers ontdekken hoe licht elektronen in metaal exciteert  Welk seizoen is het beste om Constellation Orion te observeren?
Welk seizoen is het beste om Constellation Orion te observeren?  Heeft de Galileo-missie leven op aarde gevonden?
Heeft de Galileo-missie leven op aarde gevonden?  Wat voor soort sedimentaire rots is gemaakt van de overblijfselen van organismen of fossielen?
Wat voor soort sedimentaire rots is gemaakt van de overblijfselen van organismen of fossielen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

