
Wetenschap
De faseovergangen van butaan begrijpen:de rol van intermoleculaire krachten
* Moleculaire structuur: Butaan is een koolwaterstof met een relatief eenvoudige, lineaire structuur. De enige aanwezige intermoleculaire krachten zijn van der Waals-krachten , met name de verspreidingstroepen in Londen. Deze krachten zijn zwak en komen voort uit tijdelijke fluctuaties in de elektronenverdeling binnen de moleculen.
* Laag molecuulgewicht: Butaan heeft een laag molecuulgewicht (58 g/mol). Kleinere moleculen hebben een kleiner oppervlak, wat betekent dat ze zwakkere London-dispersiekrachten ervaren in vergelijking met grotere moleculen.
* Kookpunt: De zwakke intermoleculaire krachten in butaan leiden tot een relatief laag kookpunt (ongeveer -0,5 °C of 31,3 °F). Dit betekent dat er slechts een kleine hoeveelheid energie nodig is om deze krachten te overwinnen en ervoor te zorgen dat butaan overgaat van een vloeistof naar een gas.
In contrast: Stoffen met sterke intermoleculaire krachten zoals waterstofbinding (bijvoorbeeld water) hebben veel meer energie nodig om van fase te veranderen. Daarom heeft water een veel hoger kookpunt dan butaan.
Samenvatting: De combinatie van zwakke intermoleculaire krachten en een laag molecuulgewicht maakt butaan gemakkelijk gevoelig voor faseveranderingen. Dit is de reden waarom het vaak wordt gebruikt in lichtere vloeistoffen en andere toepassingen waarbij een gemakkelijk verdampbare brandstof nodig is.
 Vindt saltatoire geleiding plaats vanwege de aanwezigheid van zout NaCl rond het neuron?
Vindt saltatoire geleiding plaats vanwege de aanwezigheid van zout NaCl rond het neuron?  Natriumhydroxide wordt gevonden in Walmart?
Natriumhydroxide wordt gevonden in Walmart?  Wat is de concentratie chloride -ion in een calciumchloride van 2,0 m oplossing?
Wat is de concentratie chloride -ion in een calciumchloride van 2,0 m oplossing?  Wat is de moleculaire formule voor 2-butyne?
Wat is de moleculaire formule voor 2-butyne?  Wanneer twee atomen combineren door elektronen over te dragen, wat voor soort binding?
Wanneer twee atomen combineren door elektronen over te dragen, wat voor soort binding?
Hoofdlijnen
- Welke populatiestructuren maximaliseren de evolutionaire fitheid?
- Welke dieren hebben witte sclera?
- Essentiële functies van levende cellen:een uitgebreid overzicht
- Wat is er zo speciaal aan een gespecialiseerde sonde?
- Waarom denk je dat cellen zo gespecialiseerd en complex zijn in plantendieren?
- Wat zijn de drie plantachtige stoffen die hun eigen voedsel produceren?
- Wat is wetenschappelijk aan make-up?
- Een stof die over een celmembraan beweegt zonder de energie te gebruiken, bewegen de neiging om te bewegen?
- Is bacteriën een voorbeeld van eukaryotische cellen?
- Het strakste niet-aminoglycoside-ligand voor de bacteriële ribosomale RNA A-site
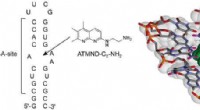
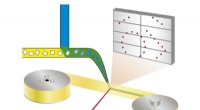
- Moleculaire schatkaarten om nieuwe materialen te ontdekken

- Nieuwe methode maakt geautomatiseerd snel onderzoek van enzymatische processen mogelijk
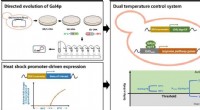
- Dubbel temperatuurregelsysteem om de biosynthese van isopreen in bakkersgist te reguleren
- On-demand glas is om de hoek

 Wat zit er in nucleïnezuren?
Wat zit er in nucleïnezuren?  Wat ontwikkelt zich wanneer een onstabiel atoom deeltjes en gammastralen afgeeft?
Wat ontwikkelt zich wanneer een onstabiel atoom deeltjes en gammastralen afgeeft?  Hoe jachtroversvliegen slachtoffers uit de lucht rukken
Hoe jachtroversvliegen slachtoffers uit de lucht rukken  Welk deeltje van een atoom heeft nul of geen lading?
Welk deeltje van een atoom heeft nul of geen lading?  Welk proces vereist membraaneiwitten maar geen energie?
Welk proces vereist membraaneiwitten maar geen energie?  Waar binnen planten breken het lichaam suiker af om energie te produceren?
Waar binnen planten breken het lichaam suiker af om energie te produceren?  Je ziet hoe je vriend een ballon over zijn trui wrijft en deze vervolgens aan de muur plakt. Om dit te onderzoeken, zet je een experiment op om te testen wat er met andere objecten gebeurt. variabele in experiment?
Je ziet hoe je vriend een ballon over zijn trui wrijft en deze vervolgens aan de muur plakt. Om dit te onderzoeken, zet je een experiment op om te testen wat er met andere objecten gebeurt. variabele in experiment?  De energie van positie zoals een rots op heuvel is welke energie?
De energie van positie zoals een rots op heuvel is welke energie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

