
Wetenschap
Alkalimetalen versus overgangsmetalen:reactiviteit uitgelegd
* Elektronenconfiguratie: Alkalimetalen hebben slechts één valentie-elektron (in de buitenste schil), dat ze gemakkelijk verliezen om een stabiel octet te bereiken. Dit maakt ze zeer reactief. Overgangsmetalen daarentegen hebben meerdere valentie-elektronen en kunnen verschillende aantallen elektronen verliezen, waardoor hun reactiviteit complexer wordt.
* Elektropositiviteit: Alkalimetalen zijn zeer elektropositief, wat betekent dat ze een sterke neiging hebben om elektronen te verliezen en positieve ionen te vormen. Hierdoor reageren ze gemakkelijk met andere elementen, vooral niet-metalen. Overgangsmetalen zijn minder elektropositief en vormen minder gemakkelijk ionen.
* Ionisatie-energie: Alkalimetalen hebben lagere ionisatie-energieën vergeleken met overgangsmetalen. Dit betekent dat het minder energie kost om een elektron uit een alkalimetaalatoom te verwijderen, waardoor ze reactiever worden.
Uitzonderingen:
Hoewel de algemene trend waar is, zijn er enkele uitzonderingen. Sommige overgangsmetalen zoals goud en platina zijn bijvoorbeeld zeer niet-reactief vanwege hun hoge ionisatie-energieën en de aanwezigheid van gevulde d-orbitalen.
Samengevat:
Hoewel er enkele uitzonderingen zijn, zijn alkalimetalen over het algemeen reactiever dan overgangsmetalen vanwege hun elektronenconfiguraties, elektropositiviteit en lagere ionisatie-energieën.
 Welke eenheid is het beste om de dichtheid van een vaste stof uit te drukken?
Welke eenheid is het beste om de dichtheid van een vaste stof uit te drukken?  Is zuurstof postitieve lading of negatief?
Is zuurstof postitieve lading of negatief?  Polymeren kunnen schade veroorzaakt door stortplaatsen verminderen
Polymeren kunnen schade veroorzaakt door stortplaatsen verminderen Wat is de relatie tussen de snelheid van een reactie en de snelheid waarmee producten worden gevormd?
Wat is de relatie tussen de snelheid van een reactie en de snelheid waarmee producten worden gevormd?  Wat zijn de verschillen tussen de watercyclus en de zuurstofcyclus?
Wat zijn de verschillen tussen de watercyclus en de zuurstofcyclus?
Hoofdlijnen
- Hoe zijn de rollen van B AN T -cellen vergelijkbaar en verschillend?
- Kunnen we een echt Jurassic Park creëren?
- Hoe raakte Alexander Fleming geïnteresseerd in biologie?
- Welke trem beschrijft de uitwisseling van genetisch materiaal tussen leden een homoloog paarchromosomen?
- Welke voordelen kan er zijn om een fabriek te hebben die meer functioneert als plantencel dan op een dierencel?
- Welk orgel regelt alle andere lichaamssystemen?
- De verschillende vormen van een eigenschap die Gene mogelijk heeft opgeroepen?
- Naarmate het klimaat warmer wordt, meer vogelnesten worden vernietigd in Finse landbouwgronden
- Wat is codominant en dominante markers?
- Hoe wordt een metaal gevormd?
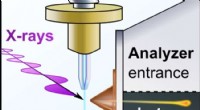
- Onderzoekers melden doorbraak in ijsafstotende materialen

- Polymeren voorkomen mogelijk gevaarlijke nevel tijdens tandartsbezoek
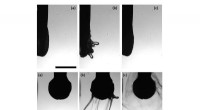
- Techniek versnelt chemische screening om prioriteit te geven aan toxiciteitstesten

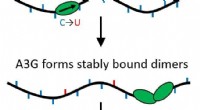
- Een als door te bewerken, twee als door wegversperring:menselijk eiwit bestrijdt HIV als monomeer en dimeer
 Wat is het bewijs voor een reactie wanneer natriumcarbonaat en zoutzuur zich vermengen?
Wat is het bewijs voor een reactie wanneer natriumcarbonaat en zoutzuur zich vermengen?  Wat is de hypothese van Wegeners?
Wat is de hypothese van Wegeners?  Hoe schrijf je 194 x 103 in wetenschappelijke notatie?
Hoe schrijf je 194 x 103 in wetenschappelijke notatie?  Moeten we killer robots verbieden?
Moeten we killer robots verbieden? Chemici gebruiken lichtenergie om kleine moleculaire ringen te produceren
Chemici gebruiken lichtenergie om kleine moleculaire ringen te produceren Wat gebeurt er met de aardkorst na een aardbeving?
Wat gebeurt er met de aardkorst na een aardbeving?  Wat zijn twee manieren waarop een berg wordt gevormd?
Wat zijn twee manieren waarop een berg wordt gevormd?  Modellering van lawinebescherming in bossen
Modellering van lawinebescherming in bossen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

