
Wetenschap
Isotopen:overeenkomsten en verschillen verklaard
Overeenkomsten en verschillen tussen isotopen
Isotopen zijn atomen van hetzelfde element die hetzelfde aantal protonen hebben (atoomnummer) maar verschillende aantallen neutronen . Dit betekent:
Overeenkomsten:
* Dezelfde chemische eigenschappen: Isotopen van hetzelfde element hebben hetzelfde aantal protonen en elektronen, die hun chemisch gedrag bepalen. Ze zullen op dezelfde manier reageren met andere elementen.
* Hetzelfde atoomnummer: Dit is het bepalende kenmerk van een element.
* Dezelfde positie in het periodiek systeem: Alle isotopen van een element bevinden zich op dezelfde plek in het periodiek systeem.
Verschillen:
* Ander massagetal: Het massagetal is de som van protonen en neutronen. Omdat isotopen verschillende aantallen neutronen hebben, hebben ze verschillende massagetallen.
* Verschillende atomaire massa: Atoommassa is het gewogen gemiddelde van de massa's van alle isotopen van een element. Dit is de reden waarom de atoommassa’s in het periodiek systeem geen gehele getallen zijn.
* Verschillende fysieke eigenschappen: Hoewel de chemische eigenschappen hetzelfde zijn, kunnen sommige fysische eigenschappen enigszins verschillen, zoals dichtheid, smeltpunt en kookpunt.
* Verschillende nucleaire stabiliteit: Sommige isotopen zijn radioactief, wat betekent dat ze onstabiel zijn en na verloop van tijd vervallen. Andere isotopen zijn stabiel.
Hier is een voorbeeld:
* Koolstof-12: 6 protonen, 6 neutronen (stabiel)
* Koolstof-14: 6 protonen, 8 neutronen (radioactief)
Zowel koolstof-12 als koolstof-14 zijn isotopen van koolstof. Ze hebben dezelfde chemische eigenschappen, maar koolstof-14 is radioactief en heeft een ander massagetal en atoommassa.
Samengevat:
Isotopen zijn fundamenteel hetzelfde element, maar verschillen in hun aantal neutronen, wat leidt tot variaties in massagetal, atoommassa en soms nucleaire stabiliteit en fysische eigenschappen.
 Welk object in het universum heeft de grootste zwaartekracht?
Welk object in het universum heeft de grootste zwaartekracht?  Wetenschappers ontrafelen hoe en waarom Amazonebomen sterven
Wetenschappers ontrafelen hoe en waarom Amazonebomen sterven  Getijden spoelen niet altijd water naar zee, studie toont
Getijden spoelen niet altijd water naar zee, studie toont Waarom komt er rook uit een brand?
Waarom komt er rook uit een brand?  Dichtere woningen kunnen ook groener zijn:hoe Nieuw-Zeeland beter bouwt voor de biodiversiteit
Dichtere woningen kunnen ook groener zijn:hoe Nieuw-Zeeland beter bouwt voor de biodiversiteit
Hoofdlijnen
- Hoe heet een vorm van plant?
- Wat vormt een voedselsubstantie in kleine ballen en wat duwen ze erin?
- Hoe is de verdeling van cellen om kiem te creëren?
- Hoe diepzeewormen helpen om natuurlijke gassen op ijs te houden
- Wat is de reproductiemethode?
- Wie zijn wetenschapper die de cel ontdekken?
- Hoe kan een fout tijdens de transcriptie het geproduceerde eiwit beïnvloeden?
- Wat zijn scavenger carnivoren?
- Wat is het diafragma van op een microscoopcontrole?
- Innovatieve verwerking en verpakking voor veilige, hoge kwaliteit, biologische bessenproducten

- Het virtuele laboratorium van UNT-professoren kan de sleutel zijn tot het voorkomen van lekken van onderzeese oliepijpleidingen

- Wijnpoten en minibotmotoren
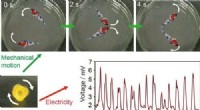
- Elektrisch op paling geïnspireerd apparaat bereikt 110 volt

- Technologie voor het produceren van aluminium matrixcomposieten uit nieuwe grondstoffen

 Welk type lucht kan meer waterdamp en Why bevatten?
Welk type lucht kan meer waterdamp en Why bevatten?  Wanneer warmte door lucht reist, is die straling?
Wanneer warmte door lucht reist, is die straling?  Wat veroorzaakt erosie van kalksteen?
Wat veroorzaakt erosie van kalksteen?  Hoe weet ik of iets een fysieke of chemische eigenschap is?
Hoe weet ik of iets een fysieke of chemische eigenschap is?  Energiebron kan op het grootste aantal gebieden worden gebruikt?
Energiebron kan op het grootste aantal gebieden worden gebruikt?  Welke invloed zal sekwestratie hebben op NASA?
Welke invloed zal sekwestratie hebben op NASA?  Wat zijn de drie vormen van wetenschapsenergie?
Wat zijn de drie vormen van wetenschapsenergie?  Niet-toxisch quantumdot-onderzoek verbetert zonnecellen
Niet-toxisch quantumdot-onderzoek verbetert zonnecellen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

