
Wetenschap
Natriumchloride versus natriumjodide:een eenvoudige oplosbaarheidstest
1. Oplosbaarheidstest:
* Water: Zowel NaCl als NaI zijn zeer oplosbaar in water. Deze test zal niet helpen ze te onderscheiden.
* Aceton: NaCl is slechts in geringe mate oplosbaar in aceton, terwijl NaI aanzienlijk beter oplosbaar is. Het oplossen van een kleine hoeveelheid kristallen in aceton zou een duidelijke indicatie opleveren. Als de kristallen gemakkelijk oplossen, is de kans groter dat het om NaI gaat. Als ze nauwelijks oplossen, is het waarschijnlijk NaCl.
2. Reactie met zilvernitraat:
* Bereid een oplossing voor: Los een kleine hoeveelheid van de kristallen op in water.
* Zilvernitraatoplossing toevoegen: Voeg een paar druppels zilvernitraat (AgNO3)-oplossing toe aan de oplossing van de kristallen.
* Observeren:
* Natriumchloride: Er zal zich een wit neerslag (AgCl) vormen.
* Natriumjodide: Er zal zich een lichtgeel neerslag (AgI) vormen.
3. Vlamtest (minder betrouwbaar):
* Een draadlus reinigen: Gebruik een schone nichroom- of platinadraadlus. Verhit de lus in de vlam van een bunsenbrander totdat deze roodgloeiend gloeit om eventuele verontreinigingen te verwijderen.
* Doop in het kristal: Dompel de lus in een kleine hoeveelheid kristallen.
* Verhitten in de vlam: Houd de lus in de vlam van de bunsenbrander.
* Observeren:
* Natriumchloride: Een heldere geeloranje vlam.
* Natriumjodide: Een zwakke geeloranje vlam, vaak gemaskeerd door het blauw van de vlam van de bunsenbrander.
Belangrijke opmerkingen:
* Veiligheid: Draag altijd een geschikte veiligheidsbril bij het uitvoeren van chemische experimenten.
* Kleinschalig: Voer deze tests op kleine schaal uit.
* Bevestiging: Als u het niet zeker weet, gebruik dan meerdere tests ter bevestiging.
Laat het me weten als je meer informatie wilt over een van deze methoden.
 COVID-19-crisis veroorzaakt 17% daling van de wereldwijde CO2-uitstoot:studie
COVID-19-crisis veroorzaakt 17% daling van de wereldwijde CO2-uitstoot:studie Beschermde gebieden kunnen de nationale economie van Brazilië helpen stimuleren, studie vondsten
Beschermde gebieden kunnen de nationale economie van Brazilië helpen stimuleren, studie vondsten Afbeelding:verwoestende Kincaid-brand in Californië blijft zich verspreiden
Afbeelding:verwoestende Kincaid-brand in Californië blijft zich verspreiden Hoe komen vissen in nieuwe vijvers?
Hoe komen vissen in nieuwe vijvers?  Giftige planten van de Amazone
Giftige planten van de Amazone
Hoofdlijnen
- Hoe wordt een schaaldier een krab?
- Wat zijn de 2 evolutiemodellen?
- Deze organellen die cel bestaat uit bepaalde in staat de verwijderde delen en zelfs vernietiging geheel door intracellulaire spijsverteringsenzymactie genoemd?
- Welk lichaamsgedeelte is de breadbasket?
- Hoe onderhoudt een cel homeostase?
- Wat gebeurt er in het mitochondriale membraan?
- Onderzoekers onderzoeken hoe neuronen kansverdelingen bemonsteren
- Wanneer chemicaliën van organisme naar een andere gaan door middel van links, wordt dit genoemd?
- Welke structuur verbindt de ER Golgi en ander membraangebonden organellen?
- Is azijn een betrouwbaar spinnenafweermiddel? Inzichten uit recent onderzoek

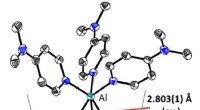
- Belangrijke mijlpaal op weg naar overgangsmetaalkatalyse met aluminium
- Zeeslakverbinding vermindert het risico op kanker

- Een manier om onderkoeling te overwinnen

- Smart label kan je op een dag laten weten wanneer je voedsel en cosmetica moet weggooien

 Wat is de volledige reactie voor fotosynthese?
Wat is de volledige reactie voor fotosynthese?  Wat is een afzetting van los materiaal gedragen en achtergelaten door Glacier klinkt als terrein?
Wat is een afzetting van los materiaal gedragen en achtergelaten door Glacier klinkt als terrein?  Welke bergen worden geassocieerd met uiteenlopende plaatgrenzen?
Welke bergen worden geassocieerd met uiteenlopende plaatgrenzen?  Cellulaire ademhaling:een energievrijgevend proces uitgelegd
Cellulaire ademhaling:een energievrijgevend proces uitgelegd  Hoe ziet de geest van niet-menselijke wezens er werkelijk uit?
Hoe ziet de geest van niet-menselijke wezens er werkelijk uit?  Wat is het verschil tussen pseudowetenschap van wetenschap en niet -wetenschap?
Wat is het verschil tussen pseudowetenschap van wetenschap en niet -wetenschap?  Wie gaf de celtheorie?
Wie gaf de celtheorie?  Wat is de primaire functie van erytrocyten?
Wat is de primaire functie van erytrocyten?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

