
Wetenschap
Goudverbindingen:onderzoek naar chemische reacties en voorbeelden
Eenvoudige samenstellingen:
* Goud(I)oxide (Au2O): Een donkerpaarse vaste stof die ontleedt bij hoge temperaturen.
* Goud(III)oxide (Au2O3): Een bruine vaste stof die onstabiel is en bij verhitting uiteenvalt in goud en zuurstof.
* Goud(I)chloride (AuCl): Een gele vaste stof die onoplosbaar is in water.
* Goud(III)chloride (AuCl3): Een roodbruine vaste stof die oplosbaar is in water en wordt gebruikt bij het raffineren en galvaniseren van goud.
* Goud(I)cyanide (AuCN): Een witte vaste stof die wordt gebruikt bij de goudextractie.
* Goud(III)cyanide (Au(CN)3): Een witte vaste stof die wordt gebruikt bij het vergulden en galvaniseren.
Complexe verbindingen:
* Goud(I)-complexen: Er zijn veel goud(I)-complexen bekend, vaak met liganden zoals cyanide, thiolaten en fosfinen. Deze complexen zijn belangrijk in de goudchemie en katalyse.
* Goud(III)-complexen: Deze complexen worden vaak aangetroffen in coördinatieverbindingen waarbij goud aan organische liganden is gebonden. Ze hebben potentiële toepassingen in de geneeskunde en katalyse.
Andere verbindingen:
* Goudamalgamen: Legeringen van goud en kwik, gebruikt in de tandheelkunde en andere toepassingen.
* Gouden intermetaalverbindingen: Legeringen van goud met andere metalen, zoals koper, zilver en platina.
Het is belangrijk op te merken dat goudverbindingen over het algemeen minder vaak voorkomen dan die van andere metalen. De hoge chemische stabiliteit van goud maakt het tot een waardevol materiaal, en de verbindingen ervan worden vaak gebruikt in gespecialiseerde toepassingen zoals katalyse, geneeskunde en elektronica.
 Is natriumacetaat oplosbaar in water?
Is natriumacetaat oplosbaar in water?  Is een legering een zuivere substantie van mengsel?
Is een legering een zuivere substantie van mengsel?  Wat is meer kans om een ionische binding te vormen een silicium en zuurstof B C koolstofwaterstof D magnesiumzuurstof?
Wat is meer kans om een ionische binding te vormen een silicium en zuurstof B C koolstofwaterstof D magnesiumzuurstof?  Wat is de vloeibare volumeformule?
Wat is de vloeibare volumeformule?  Onderzoekers creëren actief materiaal uit microscopisch kleine draaiende deeltjes
Onderzoekers creëren actief materiaal uit microscopisch kleine draaiende deeltjes
 Onderzoekers tonen aan dat grotere plantengemeenschappen productiever zijn en gevoeliger voor klimaatopwarming
Onderzoekers tonen aan dat grotere plantengemeenschappen productiever zijn en gevoeliger voor klimaatopwarming  Stadstuinen stimuleren biodiversiteit, steden duurzamer maken
Stadstuinen stimuleren biodiversiteit, steden duurzamer maken Onderzoekers proberen voedselverspilling te verminderen en de wetenschap van voedseldatum-etikettering vast te stellen
Onderzoekers proberen voedselverspilling te verminderen en de wetenschap van voedseldatum-etikettering vast te stellen Robotvloot duikt naar klimaatantwoorden in zeesneeuw
Robotvloot duikt naar klimaatantwoorden in zeesneeuw In welk type klimaat worden naaldbos gevonden?
In welk type klimaat worden naaldbos gevonden?
Hoofdlijnen
- Gebruiken dolfijnen kogelvissen voor recreatieve doeleinden?
- Is de juiste definitie van het metabolisme?
- Wat zit er in je wiet? Het zal je misschien verbazen
- Hoe diep gaat het leven? Studie beschrijft de microbiële buurt onder de oceaanbodem
- Wat zijn biologische krachten?
- Onderzoek naar het genoom van inktvissen en octopussen laat zien hoe de unieke eigenschappen van koppotigen evolueerden
- Noem twee verschillen tussen het erfelijkheidsmateriaal van een prokaryotische cel en eukaryotische cel?
- Een bacteriële cel die naar licht bewegen, zou een voorbeeld zijn van?
- Vermeld de drie belangrijkste verschillen tussen RNA en DNA?
- Drugsgebruiktrends vroeg in de COVID-19-pandemie wegspoelen

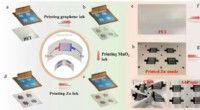
- Hoge veiligheid, flexibele en schaalbare oplaadbare planaire microbatterijen
- Oesterschelpen inspireren nieuwe methode om supersterke, flexibele polymeren

- Wetenschappers ontwikkelen innovatieve technieken voor analyse met hoge resolutie van hybride materialen
- Wetenschappers creëren een chemische methode voor het in kaart brengen van de ruimte en ontrafelen het mysterie van het getal van Mendelejev

 Afbeelding:Cassini onthult vreemde vorm van Saturnusmaan Pan
Afbeelding:Cassini onthult vreemde vorm van Saturnusmaan Pan Wat voor soort landvormen waar in het Mesozoïsche tijdperk?
Wat voor soort landvormen waar in het Mesozoïsche tijdperk?  Hoe zet je een Cosmochronotrope -klok in?
Hoe zet je een Cosmochronotrope -klok in?  Gloeit de zon door nucleaire reacties in zijn corona?
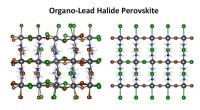
Gloeit de zon door nucleaire reacties in zijn corona?  Kijken naar atomen die bewegen in hybride perovskietkristallen onthult aanwijzingen voor het verbeteren van zonnecellen
Kijken naar atomen die bewegen in hybride perovskietkristallen onthult aanwijzingen voor het verbeteren van zonnecellen Natuurkundigen vinden een manier om geladen moleculen te controleren - met kwantumlogica
Natuurkundigen vinden een manier om geladen moleculen te controleren - met kwantumlogica H3 N2 O5 wat is het?
H3 N2 O5 wat is het?  Is het gemakkelijk om een rubberen bal te stoppen en dan van dezelfde grootte te bewegen met de snelheid?
Is het gemakkelijk om een rubberen bal te stoppen en dan van dezelfde grootte te bewegen met de snelheid?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

