
Wetenschap
Anionen in ionische binding:hoe niet-metalen negatieve ionen vormen
* Elektronegativiteit: Niet-metalen hebben een hogere elektronegativiteit dan metalen. Dit betekent dat ze een sterkere aantrekkingskracht hebben op elektronen.
* Elektronenversterking: Bij ionische binding zal een niet-metaalatoom een of meer elektronen van een metaalatoom verkrijgen om een stabiele elektronenconfiguratie te bereiken (meestal een volledige buitenschil).
* Negatieve kosten: Door het verkrijgen van elektronen wordt het niet-metaalatoom negatief geladen en vormt het een anion.
Voorbeelden van veel voorkomende niet-metaalanionen:
* Halogenen (Groep 17): Fluoride (F-), Chloride (Cl-), Bromide (Br-), Jodide (I-)
* Zuurstof (Groep 16): Oxide (O2-)
* Stikstof (Groep 15): Nitride (N3-)
* Zwavel (Groep 16): Sulfide (S2-)
* Fosfor (Groep 15): Fosfide (P3-)
Belangrijke opmerking: Hoewel de meeste anionen worden gevormd door niet-metalen, bestaan er enkele uitzonderingen. Bepaalde polyatomaire ionen kunnen bijvoorbeeld negatief geladen zijn en zowel metalen als niet-metalen bevatten.
 Jetstream wordt niet golvender ondanks de opwarming van het noordpoolgebied
Jetstream wordt niet golvender ondanks de opwarming van het noordpoolgebied Koolstofafgevende zombiebranden in veengebieden kunnen worden gedempt door nieuwe bevindingen
Koolstofafgevende zombiebranden in veengebieden kunnen worden gedempt door nieuwe bevindingen Onderzoek toont aan dat planten in Afrika groen worden voor het regenseizoen
Onderzoek toont aan dat planten in Afrika groen worden voor het regenseizoen Antarctica stevent af op een klimaatomslagpunt tegen 2060, catastrofaal smelten als de CO2-uitstoot niet snel wordt verminderd?
Antarctica stevent af op een klimaatomslagpunt tegen 2060, catastrofaal smelten als de CO2-uitstoot niet snel wordt verminderd? Verboden industrieel oplosmiddel werpt nieuw licht op methaanmysterie (update)
Verboden industrieel oplosmiddel werpt nieuw licht op methaanmysterie (update)
Hoofdlijnen
- Welke manier zijn alle levende organismen op aarde vergelijkbaar?
- Farmacie Onderzoek Onderwerpen
- Van lysosomen kan worden verwacht dat ze in cellen met grote getallen presenteren welke?
- Waarom als mens beschouwd als complex organisme?
- Wat is een chromosoom dat wordt genoemd met bijpassende informatie?
- Hoe kun je xxplain hoe de duim -eigenschap wordt bepaald met behulp van de volgende woorden allel domnate recessieve homozygote heterozygoot?
- Is nucleoli in planten- of dierencel?
- Wat is cellulaire brandstof genoemd in de biologie?
- Wat zijn de protozoa die niet in staat is tot onafhankelijke beweging?
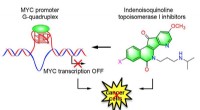
- Nieuwe antikankermiddelen kunnen de tumorgroei bij bijna elk kankertype beter onder controle houden
- Calciumverbinding breekt zoals stoot als regel af
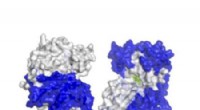
- Ontwikkeling van een enzym tegen antibioticaresistente miltvuur
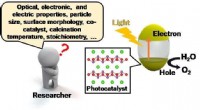
- De reis naar schone energie versnellen door optimalisatie van fotokatalysatoren
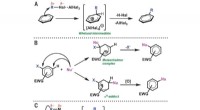
- Herbestemming van dimethyloxalylglycine om het glutaminemetabolisme te remmen
 Hoe u een besluit kunt nemen over de voor- en nadelen van kernenergie
Hoe u een besluit kunt nemen over de voor- en nadelen van kernenergie Wat vormen ammoniumfosfaat en loodnitraat?
Wat vormen ammoniumfosfaat en loodnitraat?  Wat gebeurt er de temperatuur wanneer warmte wordt geabsorbeerd door een object?
Wat gebeurt er de temperatuur wanneer warmte wordt geabsorbeerd door een object?  Welke naam wordt gegeven aan een cluster van genen met gerelateerde functies langs hun controlequenties in bacteriën?
Welke naam wordt gegeven aan een cluster van genen met gerelateerde functies langs hun controlequenties in bacteriën?  ESA's Marsrover heeft een naam - Rosalind Franklin
ESA's Marsrover heeft een naam - Rosalind Franklin Wat veroorzaakt de erosie van rotsen op het oppervlak van de manen?
Wat veroorzaakt de erosie van rotsen op het oppervlak van de manen?  Geschiedenis van vroege vestiging en overleving in de hooglanden van de Andes onthuld door oude genomen
Geschiedenis van vroege vestiging en overleving in de hooglanden van de Andes onthuld door oude genomen Hoe zijn de buitenplaneten zowel?
Hoe zijn de buitenplaneten zowel?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

