
Wetenschap
Anionen in ionische binding:niet-metaalgedrag begrijpen
* Elektronegativiteit: Niet-metalen hebben een hogere elektronegativiteit dan metalen. Dit betekent dat ze een sterkere aantrekkingskracht hebben op elektronen.
* Elektronenversterking: Wanneer een niet-metaalatoom zich bindt met een metaalatoom, heeft het de neiging een of meer elektronen te verwerven om een stabiele elektronenconfiguratie te bereiken (meestal een volledige buitenschil). Deze toename van elektronen resulteert in een negatieve lading, waardoor een anion wordt gevormd.
Voorbeelden:
* Zuurstof (O): In ionische verbindingen krijgt zuurstof vaak twee elektronen om het oxide-ion (O²⁻) te vormen.
* Chloor (Cl): Chloor krijgt één elektron en wordt het chloride-ion (Cl⁻).
* Stikstof (N): Stikstof kan drie elektronen verkrijgen om het nitride-ion (N³⁻) te vormen.
Belangrijk punt: Ionische binding omvat de overdracht van elektronen tussen atomen, wat leidt tot de vorming van tegengesteld geladen ionen (kationen en anionen). Niet-metalen zijn de elementen die doorgaans elektronen verkrijgen om anionen te vormen.
 Oroville Dam-crisis kan een teken zijn van wat komen gaat
Oroville Dam-crisis kan een teken zijn van wat komen gaat Wat zijn de verborgen voordelen van groene infrastructuur?
Wat zijn de verborgen voordelen van groene infrastructuur?  Wat zijn de overeenkomsten tussen vogels en zoogdieren?
Wat zijn de overeenkomsten tussen vogels en zoogdieren?  NASA vindt windschering die tropische cycloon Keni . dichtslaat
NASA vindt windschering die tropische cycloon Keni . dichtslaat Verdienen vulkanen of een asteroïde de schuld voor het uitsterven van dinosauriërs?
Verdienen vulkanen of een asteroïde de schuld voor het uitsterven van dinosauriërs?
Hoofdlijnen
- Welke cel maakt planten voedsel?
- Wat is het verschil tussen een protist en een menselijke huidcel?
- Welke cel wordt geïsoleerd door een vette laag?
- Welke structuur produceert bloedcellen?
- Wat is een hybride nakomelingen?
- Wetenschappers ontdekken eiwitten die stamcellen in hun ongedifferentieerde staat houden
- Wat is oorsprong van probiotica?
- Wanneer twee allelen de andere overschaduwen wat wordt aangetoond?
- Wat is het verschil tussen een bacterie en een virus?
- Chemicus creëert katalysator om anti-muggenstoffen te produceren
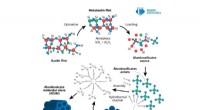
- Onderzoekers ter wereld onthullen de structuur van een belangrijk medicijndoelwit

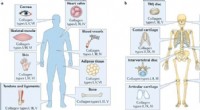
- Onderzoekers kwantificeren, karakteriseren en identificeren functies van collageen, zijn subtypes
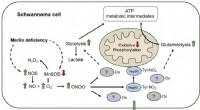
- Onderzoekers zetten belangrijke stap in de richting van kankerbehandelingen die gezonde cellen ongedeerd laten
- Technologie die RNase-activiteit detecteert

 Een uitgebreide kijk op koemelk
Een uitgebreide kijk op koemelk Rock Cycle-activiteiten voor studenten
Rock Cycle-activiteiten voor studenten Is de natuur uitsluitend linkshandig? Onderzoekers bestuderen gekoelde atomen om erachter te komen
Is de natuur uitsluitend linkshandig? Onderzoekers bestuderen gekoelde atomen om erachter te komen Hoeveel ml is gelijk aan hoe ons?
Hoeveel ml is gelijk aan hoe ons?  Hoe krijg je de energie van ATP -moleculen?
Hoe krijg je de energie van ATP -moleculen?  Hoe lang duurt het voordat een ruimteman over de maan loopt?
Hoe lang duurt het voordat een ruimteman over de maan loopt?  Wat is de zuivere stof van zwavelhexafluoride?
Wat is de zuivere stof van zwavelhexafluoride?  Gas in een kleinere container zetten beïnvloedt de dichtheid?
Gas in een kleinere container zetten beïnvloedt de dichtheid?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

