
Wetenschap
Watermolecuul-elektronenconfiguratie:alleenstaande paren begrijpen
Het watermolecuul (H₂O) heeft twee paren van niet-gebonden elektronen.
Dit is waarom:
* Valentie-elektronen van zuurstof: Zuurstof heeft zes valentie-elektronen.
* Verbinding met waterstof: Zuurstof vormt twee enkele covalente bindingen met twee waterstofatomen, met behulp van twee van zijn valentie-elektronen.
* Eenzame paren: De overige vier valentie-elektronen op zuurstof bestaan als twee paren ongebonden elektronen, ook wel alleenstaande paren genoemd.
Deze eenzame paren zijn verantwoordelijk voor de polaire aard van water en zijn vermogen om waterstofbruggen te vormen.
 Hoeveel mol fosfor bevinden zich in een 73,5 mol -oplossing P4O10?
Hoeveel mol fosfor bevinden zich in een 73,5 mol -oplossing P4O10?  Iridium en 2-methylfenantroline versnellen katalytische boryleringsreacties
Iridium en 2-methylfenantroline versnellen katalytische boryleringsreacties Wetenschappers gebruiken röntgenstralen om de geheimen van schalie te kraken, een hoeksteen van een van de snelst groeiende energiebronnen van het land
Wetenschappers gebruiken röntgenstralen om de geheimen van schalie te kraken, een hoeksteen van een van de snelst groeiende energiebronnen van het land Een veiligere manier om bacteriën in te zetten als omgevingssensoren
Een veiligere manier om bacteriën in te zetten als omgevingssensoren Waarom wordt zwaveldioxide gebruikt bij het maken van wijn?
Waarom wordt zwaveldioxide gebruikt bij het maken van wijn?
Hoofdlijnen
- Wat zit er eigenlijk in vapes? We hebben ze uit elkaar gehaald om erachter te komen
- Hoe bavianen gezonde gezinsgrenzen bewaren
- Landen in de Stille Oceaan kunnen door klimaatverandering 50 - 80% van de vis in lokale wateren verliezen
- Stroomdiagram van biotisch en abiotisch?
- Wat is de vergelijking cellulaire ademhaling?
- Leg uit hoe water verloren gaat aan de abiotische delen van de biosfeer uit biotische delen?
- Om te groeien en te overleven hebben cellen informatie nodig uit hun DNA-voedingsomgeving. Wanneer een cel echter te groot wordt, wat doet deze dan?
- Leg uit hoe enery en voedingsstoffen binnenkomen, verplaats een voedselketen in een ecosysteem?
- Is een kattencelweefsel een orgaansysteem of organisme?
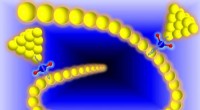
- 3D-printen verandert nanomachines in levensgrote arbeiders

- Onderzoekers creëerden een klein circuit door een enkel watermolecuul
- Algoritme gebruikt massaspectrometriegegevens om de identiteit van moleculen te voorspellen

- Elektriciteit gebruiken om verbindingen te maken voor farmaceutische producten, andere chemicaliën

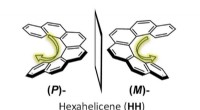
- Hoop op ontwikkeling van materialen voor 3D-displays en medische toepassingen
 Hoe steekproefgrootte te bepalen met gemiddelde en standaardafwijking
Hoe steekproefgrootte te bepalen met gemiddelde en standaardafwijking Hoe is de microscoop al jaren veranderd?
Hoe is de microscoop al jaren veranderd?  Wat zijn de sfeer van de lagen in dalende volgorde van overvloed?
Wat zijn de sfeer van de lagen in dalende volgorde van overvloed?  Wat is bewegingssnelheid?
Wat is bewegingssnelheid?  Is stikstof een metaal niet -metaal of metalloïde?
Is stikstof een metaal niet -metaal of metalloïde?  Kunstmatige fotosynthese met engineering van eiwitkristallen in bacteriën
Kunstmatige fotosynthese met engineering van eiwitkristallen in bacteriën  Droogte decimeert de belangrijkste katoenoogst in Texas
Droogte decimeert de belangrijkste katoenoogst in Texas NASA detecteert pulsen van zonnevlammen bij zon en aarde
NASA detecteert pulsen van zonnevlammen bij zon en aarde
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

