
Wetenschap
Zinkoxidatie:de reactie en de vorming van zinkoxide begrijpen
De reactie:
* Zink (Zn) + Zuurstof (O2) → Zinkoxide (ZnO)
Wat er gebeurt:
1. Oxidatie: Zink verliest elektronen (wordt geoxideerd) en wordt een positief geladen zinkion (Zn²⁺).
2. Reductie: Zuurstof krijgt elektronen (wordt gereduceerd) en wordt negatief geladen oxide-ionen (O²⁻).
3. Vorming van zinkoxide: De positief geladen zinkionen en negatief geladen oxide-ionen trekken elkaar aan en vormen een stabiele verbinding die zinkoxide (ZnO) wordt genoemd.
Kenmerken van de reactie:
* Exotherm: Bij de reactie komt warmte vrij, waardoor het metaal heet wordt.
* Vorming van een witte coating: Zinkoxide is een witte, poederachtige substantie die een beschermende laag vormt op het oppervlak van het zinkmetaal. Deze laag voorkomt verdere oxidatie en beschermt het zink tegen corrosie.
* Reactiesnelheid: De reactiesnelheid is afhankelijk van factoren zoals temperatuur, oppervlakte en de aanwezigheid van vocht.
Gebruik van zinkoxide:
Zinkoxide is een veelzijdige verbinding met tal van toepassingen, waaronder:
* Zonnebrandcrème: Gebruikt als actief ingrediënt in zonnebrandmiddelen vanwege het vermogen om UV-stralen te absorberen.
* Pigment: Gebruikt als wit pigment in verven, rubber en kunststoffen.
* Medicinale toepassingen: Wordt aangetroffen in zalven en crèmes voor de behandeling van huidaandoeningen zoals luieruitslag en acne.
* Industriële toepassingen: Gebruikt in verschillende industriële processen, waaronder de productie van rubber, lijmen en keramiek.
Samengevat: De reactie tussen zink en zuurstof resulteert in de vorming van zinkoxide, een witte beschermlaag die verdere corrosie voorkomt. Deze reactie is exotherm en heeft vele praktische toepassingen.
 Hoeveel verschillende groepen kristalstructuur zijn er in mineralen?
Hoeveel verschillende groepen kristalstructuur zijn er in mineralen?  Fysische en chemische analyse van urine?
Fysische en chemische analyse van urine?  Wat is de chemische vergelijking voor bioluminescentie?
Wat is de chemische vergelijking voor bioluminescentie?  Welke chemische stof in planten helpt zonlicht vast te houden?
Welke chemische stof in planten helpt zonlicht vast te houden?  Ontdekking versterkt de theorie dat het leven op aarde is ontstaan uit een RNA-DNA-mix
Ontdekking versterkt de theorie dat het leven op aarde is ontstaan uit een RNA-DNA-mix
 afbrokkelende wegen, Grids kosten arme landen miljarden als gevolg van stormen:Wereldbank
afbrokkelende wegen, Grids kosten arme landen miljarden als gevolg van stormen:Wereldbank Wetenschappers pleiten voor wereldwijde en lokale controle en beheer van kwik
Wetenschappers pleiten voor wereldwijde en lokale controle en beheer van kwik Atmospheric Infrared Sounder (AIRS) markeert 15 jaar zien wat er in de lucht hangt
Atmospheric Infrared Sounder (AIRS) markeert 15 jaar zien wat er in de lucht hangt Wat is de aarde in een open systeem met betrekking tot?
Wat is de aarde in een open systeem met betrekking tot?  Wat is een gecultiveerd bos?
Wat is een gecultiveerd bos?
Hoofdlijnen
- Zijn sekscellen van een mannelijk en vrouwelijk bekend als gameten?
- Wat is de theorie van hoe evolutie zich voordoet?
- Wat zijn de belangrijkste functies van sensorische organen?
- Bijdrage van celstudie door Robert Hooke?
- Wat produceren organismen?
- Zijn bonen een base of een zuur?
- Hoe bijen beslissen wat ze moeten zijn:Onderzoekers koppelen omkeerbare 'epigenetische' gedragspatronen
- Hoe slimme managers domme beslissingen nemen en waarom aandeelhouders deze aanmoedigen
- Waterige substantie die het interieur van cellen vult en organellen ophangt?
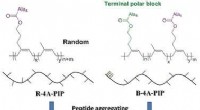
- Biomimetische strategie leidt tot sterke, recyclebaar rubber
- Nieuwe techniek voor het bestuderen van roesten van staal komt de mijnbouwsector ten goede

- Wetenschappers ontwikkelen nieuwe theorie van moleculaire evolutie

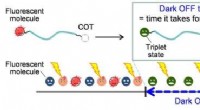
- Wanneer FRETing over kankerbiomarkers niet zal werken, focus in plaats daarvan op knipperen
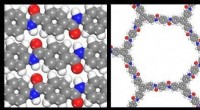
- Samenwerking leidt tot ontdekking van 2D-polymeer
 Waar chemische spijsvertering plaatsvindt:van mond tot twaalfvingerige darm
Waar chemische spijsvertering plaatsvindt:van mond tot twaalfvingerige darm  Water dat bizarre metastabiele verschijnselen vertoont wanneer het snel wordt samengeperst of afgekoeld
Water dat bizarre metastabiele verschijnselen vertoont wanneer het snel wordt samengeperst of afgekoeld Waarom hebben dierencellen geen celwand?
Waarom hebben dierencellen geen celwand?  Feiten over de aard van een tsunami
Feiten over de aard van een tsunami Wat is de vochtigheid op een berg?
Wat is de vochtigheid op een berg?  Wanneer chemie met groen licht nabootst wat er in het leven gebeurt
Wanneer chemie met groen licht nabootst wat er in het leven gebeurt  Welke richting is Mars van de aarde?
Welke richting is Mars van de aarde?  Welke adapters heb je nodig om je 240V AC aan te sluiten op een 110V AC -toevoer?
Welke adapters heb je nodig om je 240V AC aan te sluiten op een 110V AC -toevoer?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

