
Wetenschap
Chemische formule voor ijzersulfaat (FeSO₄ en Fe₂(SO₄)₃) - uitgelegd
1. Identificeer de ionen:
* IJzer kan twee gemeenschappelijke ionen vormen:
* Fe²⁺ (ferro-ion)
* Fe³⁺ (ijzerion)
* Sulfaat is een polyatomair ion met de formule SO₄²⁻ .
2. Bepaal de kosten:
* Het ferro-ion (Fe²⁺) heeft een lading van +2.
* Het ijzerion (Fe³⁺) heeft een lading van +3.
* Het sulfaation (SO₄²⁻) heeft een lading van -2.
3. Breng de kosten in evenwicht:
* Voor ijzersulfaat:
* Om de ladingen in evenwicht te brengen, hebben we één Fe²⁺-ion en één SO₄²⁻-ion nodig.
* Dit geeft ons de formule FeSO₄ .
* Voor ijzersulfaat:
* Om de ladingen in evenwicht te brengen, hebben we twee Fe³⁺-ionen en drie SO₄²⁻-ionen nodig.
* Dit geeft ons de formule Fe₂(SO₄)₃ .
Daarom hangt de chemische formule voor ijzersulfaat af van de oxidatietoestand van ijzer:
* IJzersulfaat: FeSO₄
* IJzersulfaat: Fe₂(SO₄)₃
 Is het regenwoud een van de natste plaatsen op aarde?
Is het regenwoud een van de natste plaatsen op aarde?  Wat is een milieuaspect?
Wat is een milieuaspect?  Ashouthakkers racen tegen de klok voordat kevers ze allemaal te pakken krijgen
Ashouthakkers racen tegen de klok voordat kevers ze allemaal te pakken krijgen Natuurkundigen leggen uit waarom veranderingen in het magnetische veld van de aarde zwakker zijn boven de Stille Oceaan
Natuurkundigen leggen uit waarom veranderingen in het magnetische veld van de aarde zwakker zijn boven de Stille Oceaan Hoe zich te ontdoen van Groundhogs, mollen en Gophers
Hoe zich te ontdoen van Groundhogs, mollen en Gophers
Hoofdlijnen
- Wat zijn de typen en aantallen dieren in een ecosysteem bepaald door?
- Welk orgaan produceert enzymenhormonen en een alkalische vloeistof?
- Wat is de pH van een mierenspuit?
- UA maakt deel uit van een groep die ontrafelt hoe de hersenen het geheugen beheren
- Hoe mechanische stimuli cellulaire signalering activeren
- Waarom gaan bacteriën naar de bodem van de bouilloncultuur?
- Wat betekent genetica en cosmetica?
- De pathogene protozoa die malaria veroorzaakt, wordt op mensen overgedragen?
- Onderzoekers tonen aan dat de lengte van telomeren de levensverwachting in het wild voorspellen
- Onderzoekers ontwikkelen een goedkope, gerichte antibacteriële verbinding
- Schorpioenen maken een fluorescerende stof die hen kan helpen beschermen tegen parasieten

- Bio-geïnspireerde strategieën voor de ontwikkeling van nieuwe medicijnen
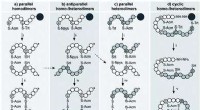
- Nieuwe keramische nanovezelsponzen kunnen worden gebruikt voor flexibele isolatie, water Zuivering

- Een nieuw facet van brandstofcelchemie
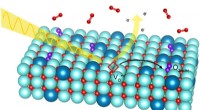
 Wat zit er in het midden van de zon?
Wat zit er in het midden van de zon?  Hoe deep learning automatische clouddetectie naar nieuwe hoogten brengt
Hoe deep learning automatische clouddetectie naar nieuwe hoogten brengt  Met plasma behandelde nanofilters helpen de wereldwatervoorziening te zuiveren
Met plasma behandelde nanofilters helpen de wereldwatervoorziening te zuiveren Het gesprek tussen plant en bodem
Het gesprek tussen plant en bodem Wat zijn de oorzaken van flikkerende sterren?
Wat zijn de oorzaken van flikkerende sterren?  Waarom stormen achtervolgen? | Hoe dingen werken
Waarom stormen achtervolgen? | Hoe dingen werken  Welk deel van een kilogram is 7 g?
Welk deel van een kilogram is 7 g?  Wat is de chemische formule voor aluminium ethanoaat?
Wat is de chemische formule voor aluminium ethanoaat?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

