
Wetenschap
Sterke versus zwakke zuren en basen:geleidbaarheid uitgelegd
De rol van ionen in elektrische geleidbaarheid
* Elektriciteit wordt getransporteerd door geladen deeltjes (ionen). In oplossingen worden deze ionen geproduceerd wanneer stoffen oplossen en dissociëren (uit elkaar vallen) in hun samenstellende ionen.
* Sterke zuren en basen ioniseren volledig in oplossing. Dit betekent dat ze een hoge concentratie vrije ionen genereren.
* Zwakke zuren en basen ioniseren slechts gedeeltelijk in oplossing. Ze creëren een veel lagere concentratie vrije ionen.
De verbinding met geleidbaarheid
* Hoge ionenconcentratie =Hoge geleidbaarheid. Hoe meer ionen er in een oplossing aanwezig zijn, hoe gemakkelijker het is voor een elektrische stroom om er doorheen te stromen.
* Lage ionenconcentratie =lage geleidbaarheid. Een oplossing met minder ionen biedt meer weerstand tegen de stroom van elektriciteit.
Voorbeeld
* Zoutzuur (HCl) is een sterk zuur. Wanneer het oplost in water, valt het volledig uiteen in H+ en Cl-ionen. Hierdoor ontstaat een hoge concentratie ionen, wat leidt tot een hoge geleidbaarheid.
* Azijnzuur (CH3COOH) is een zwak zuur. Het ioniseert slechts gedeeltelijk in oplossing en produceert een kleiner aantal H+- en CH3COO--ionen. De lagere ionenconcentratie resulteert in een lagere geleidbaarheid.
Samenvatting
Het belangrijkste verschil tussen sterke en zwakke zuren/basen ligt in hun mate van ionisatie. Sterke zuren en basen genereren een veel grotere hoeveelheid vrije ionen, waardoor een efficiënte elektrische geleiding mogelijk is. Zwakke zuren en basen produceren door hun beperkte ionisatie minder ionen, wat resulteert in een slechtere elektrische geleidbaarheid.
 Wat zijn de twee manieren om enzymactiviteit te remmen?
Wat zijn de twee manieren om enzymactiviteit te remmen?  Fosforpentafluoride (PF5):naam en chemische samenstelling
Fosforpentafluoride (PF5):naam en chemische samenstelling  Waar is de massa naar een chemische reactie gevonden?
Waar is de massa naar een chemische reactie gevonden?  J.J. Thomson:Pionier van de moderne atoomtheorie
J.J. Thomson:Pionier van de moderne atoomtheorie  Wat gebruiken wetenschappers om te beslissen of een stof een element of verbinding is?
Wat gebruiken wetenschappers om te beslissen of een stof een element of verbinding is?
 Wereldwijd netwerk dat onderzoek naar tropische bossen transformeert
Wereldwijd netwerk dat onderzoek naar tropische bossen transformeert Hoe zal de opwarming van de aarde de herfst beïnvloeden?
Hoe zal de opwarming van de aarde de herfst beïnvloeden?  Groenere brandstoffen maken de scheepvaart misschien niet veiliger - hier is waarom
Groenere brandstoffen maken de scheepvaart misschien niet veiliger - hier is waarom Nieuwe bloedtest onthult vatbaarheid voor kostbare ziekten bij melkkoeien
Nieuwe bloedtest onthult vatbaarheid voor kostbare ziekten bij melkkoeien Droogte en herstel in Californië dagen de kansen van meerdere eeuwen uit
Droogte en herstel in Californië dagen de kansen van meerdere eeuwen uit
Hoofdlijnen
- Microbiële classificatie:voorbij het 5-Koninkrijk-systeem
- Wolven bleken meer coöperatief te zijn met hun eigen soort dan honden met die van hen
- Waarom worden enzymen beschouwd als Songior in vergelijking met andere gekatalyseerde?
- Kunnen celstructuren worden gezien onder lichtmicroscopen?
- Welk deel van het menselijk lichaam exporteert eiwitten?
- Wat gebeurt er na transcriptie om het nieuwe eiwitmolecuul te produceren?
- Wat hebben planten die dieren nodig en waarom?
- Biologen werpen licht op hoe cellen hulpbronnen verplaatsen
- Een phylum wordt altijd geassocieerd?
- In het laboratorium gekweekte versus natuurlijke diamanten:deskundige gids om de verschillen te ontdekken

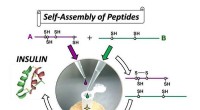
- Hoogrenderende synthese van insuline door op zelfassemblage gebaseerde organische chemie
- Nobelprijswinnende Japanse chemicus sterft op 85

- Energieonderzoekers bedenken foutloze katalysatoren

- Watermoleculen zijn goud voor nanokatalyse

 NASA ziet orkaan Walaka het Papahanaumokuakea Marine National Monument aantasten
NASA ziet orkaan Walaka het Papahanaumokuakea Marine National Monument aantasten Hoeveel landen hebben missies in de maan gehad wanneer deze reismaan?
Hoeveel landen hebben missies in de maan gehad wanneer deze reismaan?  Een reuzensprong voor microplastics
Een reuzensprong voor microplastics Wat zijn broomoxidegetallen?
Wat zijn broomoxidegetallen?  Dunne films voor efficiëntere zonnecellen
Dunne films voor efficiëntere zonnecellen Hoe wordt het genoemd als een gas rechtstreeks naar vast gaat?
Hoe wordt het genoemd als een gas rechtstreeks naar vast gaat?  Essentiële tweets van werknemers tonen verrassende positiviteit tijdens een pandemie
Essentiële tweets van werknemers tonen verrassende positiviteit tijdens een pandemie  Puerto Rico is niet hersteld van orkaan Maria
Puerto Rico is niet hersteld van orkaan Maria
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

