
Wetenschap
ClF₅:covalent of iconisch? De Bond begrijpen
* Verschil in elektronegativiteit: Chloor en fluor hebben een significant verschil in elektronegativiteit. Fluor is het meest elektronegatieve element, terwijl chloor ook behoorlijk elektronegatief is. Dit verschil in elektronegativiteit leidt tot de vorming van polaire covalente bindingen.
* Verbindende aard: De elektronen worden gedeeld tussen de chloor- en fluoratomen, maar de gedeelde elektronen worden sterker naar de fluoratomen getrokken, waardoor een polaire covalente binding ontstaat.
* Niet-metaal versus niet-metaal: Zowel chloor als fluor zijn niet-metalen. Covalente bindingen worden doorgaans gevormd tussen niet-metalen.
Belangrijke opmerking: Hoewel ClF₅ overwegend covalent is, kan het aanzienlijke verschil in elektronegativiteit ervoor zorgen dat het zich bij sommige reacties als een zwakke ionische verbinding gedraagt.
 Waarom zou een heet en vochtig klimaat de grond beïnvloeden?
Waarom zou een heet en vochtig klimaat de grond beïnvloeden?  Dodentol in plotselinge overstromingen in Turkije stijgt tot 27
Dodentol in plotselinge overstromingen in Turkije stijgt tot 27 Genieten van het uitzicht? Hoe computerspellen kunnen helpen bij het evalueren van landschappen
Genieten van het uitzicht? Hoe computerspellen kunnen helpen bij het evalueren van landschappen Hoe verhouden pesticiden en meststoffen zich tot waterbehoud?
Hoe verhouden pesticiden en meststoffen zich tot waterbehoud?  Waarom stijgt hetelucht en koelt het koud?
Waarom stijgt hetelucht en koelt het koud?
Hoofdlijnen
- Wildlife betaalt de prijs van illegale begrazing in Kenia
- Wat gebeurt er nadat u een wortel in zout water hebt gestopt?
- Verschillen tussen codering en sjabloonstrengen
- Eiwitten in haaientanden kunnen een aanwijzing zijn voor wat ze eten
- Wetenschappers tonen aan dat ribosomen een onverwachte rol spelen bij de vorming van bloedvaten
- Nieuwe aanwijzingen waarom er zo weinig antimaterie in het universum is
- Wat is studie in geïntegreerde wetenschap?
- Hoe een paar goede appels de topvariëteiten van vandaag voortbrachten, en waarom veredelaars zich moesten uitbreiden
- Hoe produceert evolutie nieuwe soorten?
- De zuurtest doorstaan:nieuw systeem met lage pH recyclet meer koolstof in waardevolle producten

- N-heterocyclische fosfines:veelbelovende katalysatoren voor transferhydrogenering
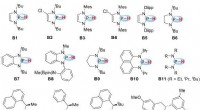
- Chemici benutten de kracht van licht om asymmetrische moleculen aan te pakken

- Veilig opslaan van puur cesium:veiligheidsnormen en beste praktijken

- Energie opslaan met eierschalen

 Versnelling vindt plaats wanneer?
Versnelling vindt plaats wanneer?  De eerste 3D-beelden van de oudste christelijke kerk in Rusland verkregen via muon-radiografie
De eerste 3D-beelden van de oudste christelijke kerk in Rusland verkregen via muon-radiografie Een vetzuur dat alle mogelijke waterstofatomen bindt aan elk koolstofatoom zou zijn?
Een vetzuur dat alle mogelijke waterstofatomen bindt aan elk koolstofatoom zou zijn?  Alcohol scheiden van water
Alcohol scheiden van water Sommige steden in Californië denken dat ze veilig zijn voor zeespiegelstijging. Zij zijn niet, nieuw onderzoek toont aan
Sommige steden in Californië denken dat ze veilig zijn voor zeespiegelstijging. Zij zijn niet, nieuw onderzoek toont aan Waar houdt zwavel graag mee?
Waar houdt zwavel graag mee?  Een momentopname van smeltend Arctisch zee-ijs in de zomer van 2018
Een momentopname van smeltend Arctisch zee-ijs in de zomer van 2018 Welk orgaan in een foetale pug verwijdert stikstofafval uit het bloed?
Welk orgaan in een foetale pug verwijdert stikstofafval uit het bloed?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

