
Wetenschap
Natrium versus chloor Atoomgrootte in NaCl:Ionische binding begrijpen
* Ionische binding: In NaCl verliest natrium een elektron om een positief geladen natriumion (Na⁺) te worden, terwijl chloor een elektron krijgt om een negatief geladen chloride-ion (Cl⁻) te worden. Deze overdracht van elektronen vormt een ionische binding.
* Effectieve nucleaire lading: Wanneer natrium zijn buitenste elektron verliest, heeft het nu minder elektronen en hetzelfde aantal protonen (positieve ladingen in de kern). Dit betekent dat de resterende elektronen sterker door de kern worden aangetrokken, wat resulteert in een kleinere ionenstraal .
* Elektronenafscherming: Chloor daarentegen krijgt een elektron. Dit toegenomen aantal elektronen verhoogt de elektron-elektronenafstoting, waardoor de elektronenwolk groter wordt. Bovendien gaat het extra elektron naar een hoger energieniveau, waardoor de omvang verder toeneemt.
Samengevat: Het verlies van een elektron in natrium leidt tot een *sterkere* aantrekkingskracht tussen de resterende elektronen en de kern, wat resulteert in een kleinere ionenstraal. De winst van een elektron in chloor leidt tot een *zwakkere* aantrekkingskracht tussen de elektronen en de kern, wat resulteert in een grotere ionenstraal.
 Chemische bindingen begrijpen:definitie en belangrijkste kenmerken
Chemische bindingen begrijpen:definitie en belangrijkste kenmerken  Zilvernitraat- en carbonaatreactie:een verklaring van chemische neerslag
Zilvernitraat- en carbonaatreactie:een verklaring van chemische neerslag  Wat voor soort reactie is cyclohexeen en broom?
Wat voor soort reactie is cyclohexeen en broom?  Chemische samenstelling van zuiveringszout:natriumbicarbonaat begrijpen
Chemische samenstelling van zuiveringszout:natriumbicarbonaat begrijpen  Welk effect heeft honing op zuiveringszout?
Welk effect heeft honing op zuiveringszout?
 Klimaatprojecties suggereren dat de maïsopbrengsten van Lancaster County in 2050 in gevaar komen
Klimaatprojecties suggereren dat de maïsopbrengsten van Lancaster County in 2050 in gevaar komen Zijn bugs mensen lastig of andersom? Onderzoek brengt enkele verrassingen aan het licht
Zijn bugs mensen lastig of andersom? Onderzoek brengt enkele verrassingen aan het licht  Amazonebossen houden de klimaatverandering niet bij
Amazonebossen houden de klimaatverandering niet bij Met een daling van LA's vervuiling door aerosolen, vegetatie komt naar voren als belangrijke bron
Met een daling van LA's vervuiling door aerosolen, vegetatie komt naar voren als belangrijke bron Hoe het veranderen van de voedselsystemen van de wereld kan helpen om de planeet te beschermen
Hoe het veranderen van de voedselsystemen van de wereld kan helpen om de planeet te beschermen
Hoofdlijnen
- Als het proces van het gebruik van een cellen om een nieuw lichaamsdeel te laten groeien dat kan worden gebruikt als natuurlijke prothese, wat wordt genoemd?
- Gestresste stokstaartjes helpen minder snel groep
- Produceert sponsachtig bot rode bloedcellen?
- Wat is het enige orgaan in het menselijk lichaam dat in staat is zichzelf te regenereren?
- Wat zijn de dingen die alle plantencellen hebben?
- Hoe een microbiële bioraffinaderij genen reguleert
- Wetenschappers ontdekken dat darmbacteriën in bijen antibioticaresistente genen naar elkaar verspreiden
- Wat is de wetenschap achter een DNA -test?
- Wat is de wetenschappelijke naam van Marigold?
- Veelzijdig, snelle en betrouwbare SARS-CoV-2-antilichaamtest

- Inzetstuk voor gezichtsmaskers kan helpen bij het diagnosticeren van ziektetoestanden, studie toont

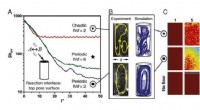
- Chaotische stromen en de oorsprong van het leven
- Bioplastics in het duurzaamheidsdilemma

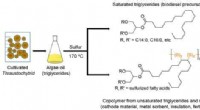
- Eenvoudige methode om hoogwaardige bioactieve stoffen te extraheren uit eencellige algenolie
 Als de maan op een asteroïde leek, welke theorie zou het meest worden ondersteund?
Als de maan op een asteroïde leek, welke theorie zou het meest worden ondersteund?  Heeft een gematigd bos naaldbomen?
Heeft een gematigd bos naaldbomen?  Heeft een object met momentum altijd energie?
Heeft een object met momentum altijd energie?  Webarchief met astronomische fotografische platen gaat online
Webarchief met astronomische fotografische platen gaat online Waarom zijn sedimentaire rotsen de enigen die fossielen bevatten?
Waarom zijn sedimentaire rotsen de enigen die fossielen bevatten?  Zijn eiwitten samengesteld uit gevouwen ketens -moleculen die animozuren worden genoemd?
Zijn eiwitten samengesteld uit gevouwen ketens -moleculen die animozuren worden genoemd?  Wat is de kracht x verplaatsing?
Wat is de kracht x verplaatsing?  Apple's smartwatch:actueel idee of uitgeklokt?
Apple's smartwatch:actueel idee of uitgeklokt?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

