
Wetenschap
Waarom is calcium hoger dan natrium in elektrochemische series?
Hier is de uitsplitsing:
* Elektrochemische serie: Deze serie vermeldt elementen (voornamelijk metalen) op basis van hun neiging om elektronen (reductie) te winnen of elektronen te verliezen (oxidatie).
* Reductiepotentieel: Een maat voor hoe waarschijnlijk een element is om elektronen te winnen en een negatief geladen ion te worden.
* Meer negatieve reductiepotentieel =gemakkelijker oxidatie: Elementen met meer negatieve reductiepotentialen zijn gemakkelijker te oxideren (verliezen elektronen).
In de elektrochemische serie heeft calcium een meer negatief reductiepotentieel dan natrium. Dit betekent dat calcium gemakkelijker wordt geoxideerd dan natrium. Dit is waarom:
* Atomische structuur: Calcium heeft twee valentie -elektronen, terwijl natrium er maar één heeft. Dit maakt het voor calcium gemakkelijker om elektronen te verliezen en een +2 ion te worden.
* Elektrostatische aantrekkingskracht: De grotere omvang van het calcium +2 ion vergeleken met het ionen van natrium +1 leidt tot een zwakkere elektrostatische aantrekkingskracht tussen het kation en zijn elektronen.
Dus, hoewel het niet strikt correct is om te zeggen dat calcium "hoger" is dan natrium, is het nauwkeuriger om te zeggen dat calcium een meer negatief reductiepotentieel heeft en daarom gemakkelijker wordt geoxideerd.
Laat het me weten als je nog meer vragen hebt!
 Meer dan een half miljoen koralen vernietigd door baggeren in de haven van Miami, studie vondsten
Meer dan een half miljoen koralen vernietigd door baggeren in de haven van Miami, studie vondsten Welke term in de wetenschap is van toepassing op een algemeen geaccepteerd verklarende idee dat brede reikwijdte is en wordt ondersteund door grote hoeveelheden bewijsmateriaal?
Welke term in de wetenschap is van toepassing op een algemeen geaccepteerd verklarende idee dat brede reikwijdte is en wordt ondersteund door grote hoeveelheden bewijsmateriaal?  Waarschuwingsstatus vulkanen Bali verlaagd na verminderde activiteit
Waarschuwingsstatus vulkanen Bali verlaagd na verminderde activiteit Broeikasgasgegevens diepe duik bereikt nieuw niveau van redelijk en waar
Broeikasgasgegevens diepe duik bereikt nieuw niveau van redelijk en waar Simulaties onthullen hoe zout water zich gedraagt in de aardmantel
Simulaties onthullen hoe zout water zich gedraagt in de aardmantel
Hoofdlijnen
- Krokodillentranen? Onderzoeksresultaten kunnen helpen de populatieomvang van bedreigde diersoorten te vergroten
- Wat is de theorie van overerving dat genen zich bevinden op chromosomen die segregatie en onafhankelijk assortiment ondergaan?
- Onderzoekers vinden dat de voorouder van algen de sleutel is tot de verspreiding van dodelijke ziekteverwekkers
- Uit onderzoek blijkt hoe gemakkelijk het is om iemands identiteit vast te stellen met mobiele telefoongegevens
- Wilt u dat luidruchtige mijnwerkers minder despotisch zijn? Denk twee keer na voordat je je tuin vult met nectarrijke bloemen
- Hoge niveaus van giftig kwik in sommige soorten haaienvlees, vinnen vormen een gevaar voor de menselijke gezondheid
- Welke bestaat uit vergelijkbare typencellen en voert een specifieke functie uit?
- Bestaan hypoallergene katten überhaupt? Drie mythen over kattenallergieën ontkracht
- Wat is CO -onderzoeker?
- Niet alleen brood en bier:microben kunnen koolstofdioxide fermenteren om ook brandstof te maken
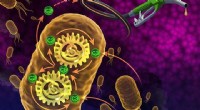
- Snelle en nauwkeurige meerkleurenbeeldvorming van biomoleculen nu mogelijk
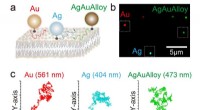
- Nieuwe zenuwgasdetector gebouwd met lego's en een smartphone

- Chemici remmen een kritische versnelling van celonsterfelijkheid
- Blauwe gaten brengen vergeten scheikundige elementen terug op het podium
 Wat is een elektrische pull -box?
Wat is een elektrische pull -box?  Methaanbronnen in Parijs in kaart brengen
Methaanbronnen in Parijs in kaart brengen Snel, niet zo woedend? Europa worstelt met elektrische scooters
Snel, niet zo woedend? Europa worstelt met elektrische scooters Evacuaties breiden zich uit in Oregon terwijl vuur zich grillig verspreidt
Evacuaties breiden zich uit in Oregon terwijl vuur zich grillig verspreidt Welke hoofdreeks zijn de slimste?
Welke hoofdreeks zijn de slimste?  Nieuw onderzoek onderzoekt hoe ziekten zich verspreiden bij primaten
Nieuw onderzoek onderzoekt hoe ziekten zich verspreiden bij primaten  Jackson Pollock, kunstenaar en natuurkundige?
Jackson Pollock, kunstenaar en natuurkundige?  Onderzoek kan ertoe bijdragen dat flexibele technologie langer meegaat, vermijd kritieke storingen
Onderzoek kan ertoe bijdragen dat flexibele technologie langer meegaat, vermijd kritieke storingen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

