
Wetenschap
Berekening van de productie van aluminiumoxide:een gids voor stoichiometrie
* Wat is de andere reactant? Aluminiumoxide ontstaat uit een reactie tussen aluminium en zuurstof. Om de geproduceerde hoeveelheid aluminiumoxide te bepalen, moet u weten hoeveel zuurstof er aanwezig is.
* Wat is de reactievergelijking? Als we de uitgebalanceerde chemische vergelijking kennen, kunnen we de stoichiometrie van de reactie berekenen.
Bijvoorbeeld:
Als de reactie is:
4 Al + 3 O₂ → 2 Al₂O₃
En je hebt 6,4 gram aluminium (Al) , kunnen we deze stappen volgen:
1. Convert gram aluminium om in mol:
- Bereken de molaire massa van aluminium (Al):26,98 g/mol
- Deel de massa van aluminium door zijn molaire massa:6,4 g / 26,98 g/mol =0,237 mol Al
2. Gebruik de molverhouding uit de uitgebalanceerde vergelijking:
- Uit de vergelijking blijkt dat 4 mol Al reageert en 2 mol Al₂O₃ vormt.
- De molverhouding is 4:2 of 2:1 (vereenvoudigd).
- Daarom zal 0,237 mol Al 0,237 mol / 2 =0,119 mol Al₂O₃ produceren.
3. Molen aluminiumoxide omzetten in grammen:
- Bereken de molaire massa van aluminiumoxide (Al₂O₃):101,96 g/mol
- Vermenigvuldig het aantal mol Al₂O₃ met de molaire massa:0,119 mol * 101,96 g/mol =12,17 gram Al₂O₃
Vul de ontbrekende informatie in, zodat ik u het juiste antwoord kan geven.
 4 gassen geproduceerd door menselijke activiteiten?
4 gassen geproduceerd door menselijke activiteiten?  Welke verklaring beschrijft het beste de vorming van een oplossing?
Welke verklaring beschrijft het beste de vorming van een oplossing?  Inzicht in oxidatiegetallen:een uitgebreide gids
Inzicht in oxidatiegetallen:een uitgebreide gids  Onderzoekers ontwikkelen thermo-responsieve eiwithydrogel
Onderzoekers ontwikkelen thermo-responsieve eiwithydrogel Wat is de molariteit van de oplossing die wordt verkregen als 26,3 g kaliumbromide wordt verdund tot 487 ml?
Wat is de molariteit van de oplossing die wordt verkregen als 26,3 g kaliumbromide wordt verdund tot 487 ml?
Hoofdlijnen
- De machtige Banyan-boom kan eeuwenlang lopen en leven
- Hoe kan de evolutie van een kenmerk binnen de ene soort een andere soort beïnvloeden?
- Wetenschappers ontdekken bossen die de klimaatverandering kunnen weerstaan
- Hebben amfibieën en zoogdieren afgedwaald van reptielen?
- Wat is celinductie?
- Welke organellen bevatten DNA?
- Wat beschrijft het beste de locatie van DNA in een bacterie?
- Zou dit bacteriële roofdier kunnen worden ingezet om biofilms op te ruimen?
- Hoe genotype en fenotype het menselijk uiterlijk en de gezondheid bepalen
- Belangrijke mijlpaal op weg naar overgangsmetaalkatalyse met aluminium
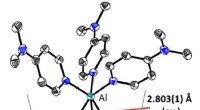
- Wetenschappers ontwikkelen vulmiddelskelet met ijsmatrijs met verbeterde thermische geleidbaarheid

- Carbonitride-aerogels bemiddelen de fotokatalytische omzetting van water
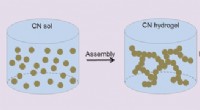
- Bloemachtige nanostructuren in natriumbatterijen

- Onderzoek details regulering van een multi-drug transporter

 T-Mobile schaft datalimieten af, maar gaat u geld besparen?
T-Mobile schaft datalimieten af, maar gaat u geld besparen?  Nieuw bewijs laat zien hoe zware elementen zijn ontstaan na de oerknal
Nieuw bewijs laat zien hoe zware elementen zijn ontstaan na de oerknal Wanneer chemische reacties optreden, worden de zaken geconserveerd, legt uit wat dat betekent?
Wanneer chemische reacties optreden, worden de zaken geconserveerd, legt uit wat dat betekent?  De verborgen gegevens in uw vingerafdrukken
De verborgen gegevens in uw vingerafdrukken Quiz over het introduceren van cellen met antwoorden?
Quiz over het introduceren van cellen met antwoorden?  Wat zijn enkele van de veldenwetenschap waaraan de evolutionaire biologie bijdraagt?
Wat zijn enkele van de veldenwetenschap waaraan de evolutionaire biologie bijdraagt?  Gebruik van diamantmicrodeeltjes om zeer veilige anti-namaaklabels te creëren
Gebruik van diamantmicrodeeltjes om zeer veilige anti-namaaklabels te creëren  Welke zin beschrijft een wetenschappelijke wet?
Welke zin beschrijft een wetenschappelijke wet?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

