
Wetenschap
Covalente obligaties begrijpen:hoe de bindingscapaciteit te bepalen
Hier ziet u hoe:
1. Bepaal het groepsnummer van het element: Dit is de verticale kolom waarin het element zich bevindt in het periodiek systeem.
2. Voor hoofdgroepelementen: Het groepsnummer (met uitzondering van de groepen 3-12, de overgangsmetalen) vertelt u doorgaans het aantal valentie-elektronen.
3. Elementen hebben de neiging covalente bindingen te vormen om een stabiel octet te bereiken: Dit betekent dat ze acht elektronen in hun buitenste schil willen hebben.
4. Bereken het aantal obligaties: Trek het huidige aantal valentie-elektronen van het element af van acht om te bepalen hoeveel elektronen het nog meer nodig heeft. Dit aantal is hetzelfde als het aantal covalente bindingen dat het doorgaans zal vormen.
Voorbeeld:
* Zuurstof (O): Zuurstof zit in groep 16 en heeft dus 6 valentie-elektronen. Om een octet te bereiken, heeft het nog 2 elektronen nodig (8-6=2). Daarom vormt zuurstof doorgaans twee covalente bindingen .
Uitzonderingen:
* Waterstof (H): Er zijn slechts 2 elektronen nodig voor een volledige buitenste schil, waardoor er één covalente binding ontstaat.
* Boor (B): Kan 3 covalente bindingen vormen, maar vormt er vaak slechts 2 om een stabiele configuratie van 6 elektronen te bereiken.
* Overgangsmetalen: Ze kunnen variabele oxidatietoestanden hebben en een variërend aantal covalente bindingen vormen.
Opmerking: Dit is een algemene regel en er kunnen uitzonderingen zijn, vooral bij complexere moleculen. Het begrijpen van valentie-elektronen en de octetregel is echter een goed startpunt voor het voorspellen van het aantal covalente bindingen dat een element zou kunnen vormen.
 Natuurkundigen maken een model om de eigenschappen van elk molecuul te voorspellen
Natuurkundigen maken een model om de eigenschappen van elk molecuul te voorspellen Hoeveel elektronen doneert één atoom van calcium aan zuurstof tijdens de Formation -verbinding Cao?
Hoeveel elektronen doneert één atoom van calcium aan zuurstof tijdens de Formation -verbinding Cao?  Het uitlaatgas van een elektriciteitscentrale kan worden teruggewonnen en gebruikt als grondstof voor reactie
Het uitlaatgas van een elektriciteitscentrale kan worden teruggewonnen en gebruikt als grondstof voor reactie Welk element zou je verwachten dat zich het meest als koolstof (C) gedraagt?
Welk element zou je verwachten dat zich het meest als koolstof (C) gedraagt?  De formule van een verbinding met de kleinste verhoudingen wordt genoemd?
De formule van een verbinding met de kleinste verhoudingen wordt genoemd?
 West-Siberische rivieren en meren stoten broeikasgassen uit in de atmosfeer
West-Siberische rivieren en meren stoten broeikasgassen uit in de atmosfeer Kleine rode klavermijten in uw huis begrijpen en beheren
Kleine rode klavermijten in uw huis begrijpen en beheren  Afnemende sneeuwbedekking zorgt voor toenemende methaanproductie in bevroren meren
Afnemende sneeuwbedekking zorgt voor toenemende methaanproductie in bevroren meren Het kappen van hele bomen mag de biodiversiteit van planten niet belemmeren
Het kappen van hele bomen mag de biodiversiteit van planten niet belemmeren Welke planten en dieren in het wild van Antarctica zijn op het land?
Welke planten en dieren in het wild van Antarctica zijn op het land?
Hoofdlijnen
- Wat is een mRNA -vernietiger?
- Geklede varkenskarkassen onthullen de geheimen van mummificatie; onderzoek biedt inzichten voor forensische wetenschappers
- Student onderzoekt hoe de sms-cultuur is geëvolueerd
- Een ondergrondse stengel die vaatweefsel bezit is een.?
- Waar worden enzymen geproduceerd binnen of buiten de cellen van een organisme?
- Een hydrozoan die eigenlijk een kolonie van vier soorten speciale poliepen is, hangen van elkaar af om te overleven?
- Hoe verschillen cellen van eencellige organismen van de meercellige organismen?
- Wat moet een cel doen voordat je verdeelt?
- Hoe een DNA-model te labelen
- Onderzoekers bieden inzicht in lichtgewicht materiaal dat uitzet bij warmte

- Een kankervernietigersubstantie met nieuw werkingsmechanisme gevonden

- Ingenieurs ontdekken waarom gevallen bladeren op treinrails zo glad zijn

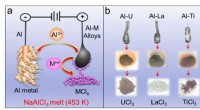
- Wetenschappers stellen IAP-proces voor voor scheiding van aluminiumlegeringen
- Onderzoekers bereiken doorbraak in 3D-geprint roestvrij staal van mariene kwaliteit

 Seksisme moet op scholen worden uitgedaagd, niet alleen werkplekken
Seksisme moet op scholen worden uitgedaagd, niet alleen werkplekken Wat omvat de procestekst in de wetenschap?
Wat omvat de procestekst in de wetenschap?  Hoe classificeren geologen kristalstracters?
Hoe classificeren geologen kristalstracters?  Is kalkwater een zuur of alkali?
Is kalkwater een zuur of alkali?  Waar begint DNA -vertaling mee?
Waar begint DNA -vertaling mee?  Welk type plaatgrenzen vormden de San Gabriel -bergen?
Welk type plaatgrenzen vormden de San Gabriel -bergen?  Noem drie gebruik voor nucleaire reacties?
Noem drie gebruik voor nucleaire reacties?  Metaal die reageert met zuren, klinkt het als Throgh, je zou je gerechten erin kunnen wassen?
Metaal die reageert met zuren, klinkt het als Throgh, je zou je gerechten erin kunnen wassen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

