
Wetenschap
Ionische versus moleculaire verbindingen:belangrijkste verschillen en eigenschappen
Ionische versus moleculaire verbindingen:een vergelijking
Hier volgt een overzicht van de belangrijkste verschillen tussen ionische en moleculaire verbindingen:
1. Verlijming:
* Ionische verbindingen: Gevormd door elektrostatische aantrekking tussen tegengesteld geladen ionen. Deze ionen worden gevormd door de volledige overdracht van elektronen van een metaal naar een niet-metaal.
* Moleculaire verbindingen: Gevormd door het delen van elektronen tussen niet-metaalatomen. Door dit delen ontstaan covalente bindingen.
2. Structuur:
* Ionische verbindingen: Vorm kristallijne structuren met zich herhalende, driedimensionale reeksen ionen.
* Moleculaire verbindingen: Bestaan vaak als discrete moleculen met specifieke geometrieën die worden bepaald door de rangschikking van atomen en hun gedeelde elektronen.
3. Fysieke eigenschappen:
| Eigendom | Ionische verbindingen | Moleculaire verbindingen |
|----------------|-----------------|------------------|
| Bewaren bij kamertemperatuur | Typisch vaste stoffen | Kunnen vaste stoffen, vloeistoffen of gassen zijn |
| Smeltpunt | Hoge smeltpunten | Lagere smeltpunten |
| Kookpunt | Hoge kookpunten | Lagere kookpunten |
| Oplosbaarheid | Vaak oplosbaar in water | Kan oplosbaar of onoplosbaar zijn in water |
| Elektrische geleidbaarheid | Goede geleiders in gesmolten toestand of opgelost in water | Slechte geleiders |
4. Voorbeelden:
* Ionische verbindingen: NaCl (keukenzout), CaCO3 (calciumcarbonaat), MgO (magnesiumoxide)
* Moleculaire verbindingen: H2O (water), CO2 (kooldioxide), CH4 (methaan)
5. Samenvatting van de belangrijkste verschillen:
| Kenmerk | Ionische verbindingen | Moleculaire verbindingen |
|----------------|-----------------|------------------|
| Verbinding | Elektrostatische aantrekking (ionische bindingen) | Covalente obligaties |
| Structuur | Kristallijn rooster | Discrete moleculen |
| Fysieke eigenschappen | Hoge smelt-/kookpunten, vaak oplosbaar in water, goede elektrische geleidbaarheid (in gesmolten toestand of oplossing) | Lagere smelt-/kookpunten, variërende oplosbaarheid in water, slechte elektrische geleidbaarheid |
Belangrijke opmerking: Sommige verbindingen kunnen kenmerken van zowel ionische als moleculaire binding vertonen, waardoor ze moeilijk definitief te categoriseren zijn. Deze worden vaak "polaire covalente" verbindingen genoemd.
Het begrijpen van de verschillen tussen ionische en moleculaire verbindingen is cruciaal voor het begrijpen van hun eigenschappen, reacties en toepassingen op verschillende gebieden, zoals scheikunde, biologie en materiaalkunde.
 Baanbrekende voedingswetenschap onthult hoe u uw borden kunt afmaken en voedselverspilling kunt verminderen
Baanbrekende voedingswetenschap onthult hoe u uw borden kunt afmaken en voedselverspilling kunt verminderen De nieuwsgierigheid van cichliden bevordert de biodiversiteit:hoe verkennend gedrag helpt bij ecologische aanpassing
De nieuwsgierigheid van cichliden bevordert de biodiversiteit:hoe verkennend gedrag helpt bij ecologische aanpassing  Geliefde 600 jaar oude witte eik maakt laatste buiging
Geliefde 600 jaar oude witte eik maakt laatste buiging Duurzame pelletproductie redt levens
Duurzame pelletproductie redt levens Het derde klimaatrapport van Oregon toont aan dat de staat nog steeds aan het opwarmen is, ondanks de koude winter
Het derde klimaatrapport van Oregon toont aan dat de staat nog steeds aan het opwarmen is, ondanks de koude winter
Hoofdlijnen
- Welke dieren hadden de biosfeer 2?
- Wat zijn de twee functies van cytoskelet?
- Welke cellen dragen voedingsstoffen?
- Welke typen zijn de mitochondria en ribosomen?
- Waarom draagt DNA de code?
- Wat is een andere naam voor een zaad opgeslagen voedsel?
- Welke levensprocessen vereisen gespecialiseerde cellen in meercellige organismen?
- Waaruit bestaat de microscoop?
- Wanneer moet u uw hond castreren om gezondheidsrisico's te voorkomen?
- Mengsels van voedselingrediënten gevoeliger voor klimaatverandering, studie vondsten

- Darmkanker en doodgeboorten voorkomen

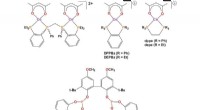
- Nieuw kobaltcomplex kan de kosten van hydroformylering verlagen
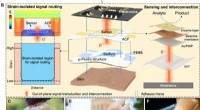
- Een draagbare, vrijstaand elektrochemisch detectiesysteem
- Hoe u een laboratoriumrapport over titratie schrijft:stapsgewijze handleiding

 Hoe groot is Afrikaanse tektonische plaat?
Hoe groot is Afrikaanse tektonische plaat?  Hoe evolutie werkt
Hoe evolutie werkt  Rode superreuzen borrelen en schuimen zo hard dat hun positie in de lucht rond lijkt te dansen
Rode superreuzen borrelen en schuimen zo hard dat hun positie in de lucht rond lijkt te dansen Heeft de binnenkant van de binnenvlaktes Mountains Hills of Plains?
Heeft de binnenkant van de binnenvlaktes Mountains Hills of Plains?  Waarom ontstaat breking van een golf wanneer het van het ene materiaal naar het andere reist?
Waarom ontstaat breking van een golf wanneer het van het ene materiaal naar het andere reist?  Welk chromosomaal erfelijk materiaal kan worden verpakt in deze organele eukaryotische cellen maar geen prokaryotische cellen?
Welk chromosomaal erfelijk materiaal kan worden verpakt in deze organele eukaryotische cellen maar geen prokaryotische cellen?  Kinderen geboren uit verkrachting:de verwoestende erfenis van seksueel geweld in Rwanda na de genocide
Kinderen geboren uit verkrachting:de verwoestende erfenis van seksueel geweld in Rwanda na de genocide  Is het of is het niet? Het Pentaquark-debat laait op
Is het of is het niet? Het Pentaquark-debat laait op
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

