
Wetenschap
Intermoleculaire krachten in boortrichloride (BCl3):Londense dispersie begrijpen
Boortrichloride (BCl3 ) is een niet-polair molecuul. Dit komt doordat de drie chlooratomen symmetrisch rond het booratoom zijn gerangschikt, wat resulteert in een molecuul zonder netto dipoolmoment.
Daarom is de dominante intermoleculaire kracht in boortrichloride Londense dispersiekrachten .
Dit is waarom:
* Londense verspreidingstroepen: Dit zijn tijdelijke, zwakke aantrekkingen die voortkomen uit tijdelijke fluctuaties in de elektronenverdeling binnen moleculen. Alle moleculen ervaren Londense dispersiekrachten, zelfs niet-polaire.
Hoewel boortrichloride geen dipool-dipoolinteracties of waterstofbindingen heeft (die sterker zijn dan de Londense dispersiekrachten), ervaart het nog steeds deze zwakke krachten vanwege de tijdelijke, geïnduceerde dipolen.
 Lily de kerkuil laat zien hoe vogels vliegen bij windstoten
Lily de kerkuil laat zien hoe vogels vliegen bij windstoten  Levenscyclus van een adelaar
Levenscyclus van een adelaar Nieuw Amerikaans onderzoek onthult dat natuurlijke oplossingen de opwarming van de aarde kunnen verminderen
Nieuw Amerikaans onderzoek onthult dat natuurlijke oplossingen de opwarming van de aarde kunnen verminderen China's oorlog tegen vervuiling laat veelbelovende resultaten zien, studie vondsten
China's oorlog tegen vervuiling laat veelbelovende resultaten zien, studie vondsten Hittegolf verschroeit Europa, van Londen naar Siberië
Hittegolf verschroeit Europa, van Londen naar Siberië
Hoofdlijnen
- Hoe komt cytokinese op in plantencellen met hoe het voor de diercel gebeurt?
- Bij dieren resulteert meiose in gameten en bemestingsresultaten wat?
- Wetenschappers onthullen dat de schedelgaten van dinosaurussen natuurlijke ventilatieopeningen waren
- Binaire splijting:hoe bacteriën zich vermenigvuldigen door zich in twee cellen te splitsen
- Als de cel actief is, heeft het min of meer mitochondria?
- De belangrijkste componenten van het skeletsysteem
- Tussen geometrie en biologie:hoe waarom is het aantal soorten afhankelijk van het gebied?
- Waarom onze hersenen kansen missen om te verbeteren door middel van aftrekken
- Hoe meiose genetische diversiteit stimuleert:belangrijke stappen en mechanismen
- Reactie-inzichten helpen bij het maken van duurzame vloeibare brandstoffen
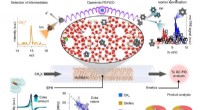
- Onderzoekers boeken vooruitgang in groene chemie met nieuwe katalysator voor reductie van koolstofdioxide

- Bakoliecoating voorkomt dat bacteriën groeien op voedselverwerkende apparatuur

- Klasse van eiwitten die betrokken zijn bij essentiële celfuncties heeft een onverwachte rol, wetenschappers ontdekken
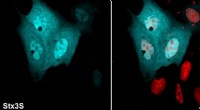
- Ontwikkeling van vereenvoudigde nieuwe massaspectrometrische techniek met behulp van laser en grafeen

 GM's nieuwste voertuig:off-road, zelfrijdende rover voor de maan
GM's nieuwste voertuig:off-road, zelfrijdende rover voor de maan Ideeën voor het maken van een 3D-model van een cel
Ideeën voor het maken van een 3D-model van een cel  Waarom een slechte klantenservice niet snel zal verbeteren
Waarom een slechte klantenservice niet snel zal verbeteren Gebruik wat voor soort energie uit je hand tot het boek als je een boek opneemt?
Gebruik wat voor soort energie uit je hand tot het boek als je een boek opneemt?  Wat is het verschil tussen NADH en NADPH?
Wat is het verschil tussen NADH en NADPH?  Hoe leraren dit najaar sociale media kunnen gebruiken om het leren te verbeteren
Hoe leraren dit najaar sociale media kunnen gebruiken om het leren te verbeteren  Nest van bedreigde reuzenweekschildpad gevonden in Cambodja
Nest van bedreigde reuzenweekschildpad gevonden in Cambodja Welk type grond kan zo harde steen worden als het opdroogt?
Welk type grond kan zo harde steen worden als het opdroogt?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

