
Wetenschap
1+ Ionen:elementen en voorbeelden identificeren - Chemie uitgelegd
Elementen die ionen vormen met een lading van 1+ zijn elementen die de neiging hebben één elektron te verliezen om een stabiele elektronenconfiguratie te bereiken. Deze elementen bevinden zich doorgaans in Groep 1 (alkalimetalen) van het periodiek systeem.
Hier zijn enkele voorbeelden:
* Lithium (Li) :Li+
* Natrium (Na) :Na+
* Kalium (K) :K+
* Rubidium (Rb) :Rb+
* Cesium (Cs) :Cs+
Opmerking: Terwijl Waterstof (H) bevindt zich ook in Groep 1 en kan zowel een 1+ ion (H+) als een 1- ion (H-) vormen.
Daarnaast enkele elementen in Groep 11 (muntmetalen) kunnen ook 1+ ionen vormen, hoewel ze minder vaak voorkomen. Bijvoorbeeld:
* Koper (Cu) kan zowel Cu+ als Cu2+ ionen vormen.
* Zilver (Ag) vormt typisch Ag+-ionen.
* Goud (au) kan zowel Au+ als Au3+ ionen vormen.
 Hoeveel atomen zijn er in jodium pentachloride?
Hoeveel atomen zijn er in jodium pentachloride?  Waarom zijn vloeistoffen slechte warmtegeleiders?
Waarom zijn vloeistoffen slechte warmtegeleiders?  Waarom wordt één enkele indicator gebruikt om de pH van de oplossing te bepalen?
Waarom wordt één enkele indicator gebruikt om de pH van de oplossing te bepalen?  Selectieve olefine-metathese met dubbele golflengte 3D-printen:hoe ingenieurs SWOMP gebruiken
Selectieve olefine-metathese met dubbele golflengte 3D-printen:hoe ingenieurs SWOMP gebruiken  Materiaal om de overgang naar schone waterstofbrandstof te helpen
Materiaal om de overgang naar schone waterstofbrandstof te helpen
 Onderzoeker doet ontdekking van diepzeekoraalriffen in de diepten van de Noord-Pacific
Onderzoeker doet ontdekking van diepzeekoraalriffen in de diepten van de Noord-Pacific De wereld wordt geconfronteerd met een wereldwijde zandcrisis
De wereld wordt geconfronteerd met een wereldwijde zandcrisis Gigantische lavakoepel bevestigd in de Japanse Kikai Caldera
Gigantische lavakoepel bevestigd in de Japanse Kikai Caldera Indonesië verhoogt vulkaanalarm Bali tot hoogste niveau
Indonesië verhoogt vulkaanalarm Bali tot hoogste niveau Hoe zien inheemse mensen eruit in het Amazon -regenwoud?
Hoe zien inheemse mensen eruit in het Amazon -regenwoud?
Hoofdlijnen
- Welk systeem omvat alle lichaamsprocessen met betrekking tot voedsel?
- Fossielen onthullen hoe oude vogels ruiden en zouden kunnen verklaren waarom moderne dinosauriërs overleefden terwijl andere dinosauriërs stierven
- Wat is biostatastiek?
- Hoe zijn eukaryotische en prokaryotische cellen zowel?
- Wat is een Sugardoodle?
- Welk systeem voert de organische functies uit van inname -digestie en uitscheiding?
- Leg uit waarom DNA -replicatie moet optreden voordat de mitose begint?
- Hoe wordt de krachtpatser van een cel genoemd omdat het voedingsstoffen afbreekt om een grote energiebroncel te maken?
- Bavianengeslachten verschillen in de manier waarop sociale status 'onder de huid' komt
- Vloeistof-vloeistof fasescheiding blijkt het proces van het omzetten van spidroïne-eiwitten in spinnenwebvezels te stimuleren
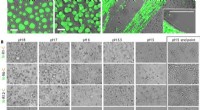
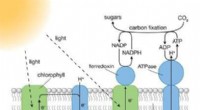
- Wetenschappers ontwerpen moleculair systeem voor kunstmatige fotosynthese
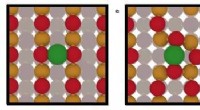
- Nieuwe strategie verbetert de stabiliteit van metaalkatalysatoren uit de platinagroep

- Nanodeeltjes in lithium-zwavelbatterijen gedetecteerd met neutronenexperiment

- Wetenschappers stellen een dynamische ladings- en oxidatietoestand voor voor katalysatoren met één atoom
 Hoe mensen de sterren in het leven gebruiken?
Hoe mensen de sterren in het leven gebruiken?  Hoe worden de grootste getijdenbewegingen genoemd?
Hoe worden de grootste getijdenbewegingen genoemd?  Wat betekent luchtweergave in de wetenschap?
Wat betekent luchtweergave in de wetenschap?  Wat zijn oplosbare en onoplosbare stoffen. Heb je elk twee voorbeeld?
Wat zijn oplosbare en onoplosbare stoffen. Heb je elk twee voorbeeld?  Nieuw mechanisme zorgt voor een lager energieverbruik voor OLED-schermen
Nieuw mechanisme zorgt voor een lager energieverbruik voor OLED-schermen Een hulpmiddel voor diepgaand leren voor gepersonaliseerde trainingsaanbevelingen uit fitness-trackinggegevens
Een hulpmiddel voor diepgaand leren voor gepersonaliseerde trainingsaanbevelingen uit fitness-trackinggegevens NASA selecteert nieuw instrument om belangrijke klimaatrecord voort te zetten
NASA selecteert nieuw instrument om belangrijke klimaatrecord voort te zetten Waarom komt de maan op en gaat hij onder waar hij dat doet?
Waarom komt de maan op en gaat hij onder waar hij dat doet?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

