
Wetenschap
Ammoniak- en waterreactie:chemische vergelijking en uitleg
NH₃(aq) + H₂O(l) ⇌ NH₄⁺(aq) + OH⁻(aq)
Hier is een overzicht:
* NH₃(aq) vertegenwoordigt ammoniak opgelost in water (waterige oplossing).
* H₂O(l) vertegenwoordigt vloeibaar water.
* NH₄⁺(aq) vertegenwoordigt het ammoniumion, gevormd wanneer ammoniak een proton (H⁺) uit water accepteert.
* OH⁻(aq) vertegenwoordigt het hydroxide-ion, gevormd wanneer water een proton verliest.
Uitleg:
Ammoniak is een zwakke base, wat betekent dat het protonen kan accepteren. In aanwezigheid van water zal een klein deel van de ammoniakmoleculen reageren met watermoleculen, waarbij ze een proton accepteren en ammoniumionen (NH₄⁺) vormen. Tegelijkertijd verliezen watermoleculen een proton en vormen ze hydroxide-ionen (OH⁻). Dit proces creëert een basische oplossing vanwege de aanwezigheid van hydroxide-ionen.
Belangrijkste punten:
*De reactie is omkeerbaar, wat betekent dat deze in beide richtingen kan verlopen.
* De evenwichtspositie bevoordeelt de reactanten (ammoniak en water) meer dan de producten (ammonium- en hydroxide-ionen). Dit betekent dat de meeste ammoniakmoleculen niet gereageerd hebben.
*De reactie is exotherm, wat betekent dat er warmte vrijkomt.
* Deze reactie is belangrijk voor het begrijpen van de eigenschappen van ammoniak als base en het vermogen ervan om zuren te neutraliseren.
 Wat gebeurt er tijdens een nucleaire reactie met de buitenste elektronen?
Wat gebeurt er tijdens een nucleaire reactie met de buitenste elektronen?  Is goud chemisch gebonden of een mengsel?
Is goud chemisch gebonden of een mengsel?  Sous-vide kookmethode maakt rundvleeseiwit beter verteerbaar
Sous-vide kookmethode maakt rundvleeseiwit beter verteerbaar Wat is een vaste stof gevormd uit de chemische reactie van twee oplossingen die worden genoemd?
Wat is een vaste stof gevormd uit de chemische reactie van twee oplossingen die worden genoemd?  Nieuwe combinatie van materialen zorgt voor recordbrekende lithium-metaalcel
Nieuwe combinatie van materialen zorgt voor recordbrekende lithium-metaalcel
 Asfalt geïdentificeerd als bron voor niet-afbreekbare koolstof- en zwavelverbindingen in de oceaan
Asfalt geïdentificeerd als bron voor niet-afbreekbare koolstof- en zwavelverbindingen in de oceaan Gluren naar het sanitair van een van de meest actieve vulkanen van de Aleoeten
Gluren naar het sanitair van een van de meest actieve vulkanen van de Aleoeten Modellen suggereren dat injectie van sulfaataerosolen in de stratosfeer onbedoelde gevolgen kan hebben
Modellen suggereren dat injectie van sulfaataerosolen in de stratosfeer onbedoelde gevolgen kan hebben Welke planten leven in de zonovergoten zone?
Welke planten leven in de zonovergoten zone?  Pacific Ocean maakt plaats voor 's werelds volgende supercontinent
Pacific Ocean maakt plaats voor 's werelds volgende supercontinent
Hoofdlijnen
- Wat zijn de delen van een dierencel en wat ze doen?
- Onderzoek benadrukt pathoblokkers als toekomstig alternatief voor antibiotica
- Hoeveel vellen papier kunnen uit één enkele boom worden geproduceerd?
- Wat is de wetenschappelijke naam van bamboe?
- Wat zijn enkele niet-voorbeelden van eiwitten?
- Wat is weefsel in een levend organisme?
- Wat is een verklaring van de wetenschappelijke methode?
- Wat is een labotamist?
- Wat is nodig voor alle organismen om het leven te ondersteunen?
- Fluorescerend polymeer detecteert sporen van explosieven

- Een chemische aanwijzing voor hoe het leven op aarde begon

- Realtime dampanalyse kan de training van explosievendetecterende honden verbeteren

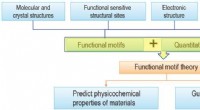
- De cruciale rol van functionele motieven—microstructurele eenheden die materiële functies bepalen—in materiaalonderzoek
- Elementverhoudingen in chemische verbindingen bepalen:een stapsgewijze handleiding

 Wat zijn interleukines?
Wat zijn interleukines?  Hoeveel atomen zijn er in de zon als alle waterstof en massa van 2 x 10 is om 30 kg A atoom 1,67 -27 kg te voeden?
Hoeveel atomen zijn er in de zon als alle waterstof en massa van 2 x 10 is om 30 kg A atoom 1,67 -27 kg te voeden?  9-Volt batterijprojecten
9-Volt batterijprojecten  Welk element ontstaat wanneer calciumhydroxide reageert met waterstoffosfaat?
Welk element ontstaat wanneer calciumhydroxide reageert met waterstoffosfaat?  Sleutelgewassen zijn de focus van landbouwonderzoek
Sleutelgewassen zijn de focus van landbouwonderzoek Hoe Zamboni's werken
Hoe Zamboni's werken  De termen stralende energie is pijnlijk en verwijst naar welke vereiste in fotosynthese?
De termen stralende energie is pijnlijk en verwijst naar welke vereiste in fotosynthese?  Onderzoek laat zien hoe de geschiedenis het succes en falen van ecologisch herstel kan beïnvloeden
Onderzoek laat zien hoe de geschiedenis het succes en falen van ecologisch herstel kan beïnvloeden
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

