
Wetenschap
Covalente obligaties begrijpen:polair versus niet-polair
* Polaire covalente obligaties: Deze bindingen ontstaan wanneer elektronen *ongelijk* worden gedeeld tussen twee atomen. Dit gebeurt omdat één atoom een sterkere aantrekkingskracht op de elektronen heeft (hogere elektronegativiteit). Hierdoor ontstaat een licht positieve lading op het ene atoom en een licht negatieve lading op het andere, wat resulteert in een dipoolmoment.
* Niet-polaire covalente obligaties: Deze bindingen ontstaan wanneer elektronen *gelijk* worden verdeeld tussen twee atomen. Dit gebeurt wanneer de twee atomen identieke of zeer vergelijkbare elektronegativiteiten hebben. Er is geen scheiding van lading en geen dipoolmoment.
Belangrijkste afhaalmaaltijden: De definitie van een covalente binding impliceert het delen van elektronen. Als het delen *niet* gelijk is, wordt het een polaire covalente binding. Daarom kan een binding niet zowel niet-polair als covalent zijn.
Wat kan de verwarring zijn?
Je denkt misschien aan zoiets als een niet-polair molecuul . Een molecuul kan niet-polair zijn, zelfs als het polaire covalente bindingen bevat, als de polariteiten elkaar opheffen vanwege de vorm van het molecuul (zoals CO2).
 Recht op voedselstrategie zou voedselverspilling op boerderijen kunnen elimineren
Recht op voedselstrategie zou voedselverspilling op boerderijen kunnen elimineren Biodiversiteit en afbraak van planten moeten worden meegenomen in klimaatmodellen, studie vondsten
Biodiversiteit en afbraak van planten moeten worden meegenomen in klimaatmodellen, studie vondsten Team voorspelt toenemende afname van hemlock als de winters warmer worden
Team voorspelt toenemende afname van hemlock als de winters warmer worden Orkanen en tyfoons:cyclonen met een andere naam
Orkanen en tyfoons:cyclonen met een andere naam Wat is observeren en vergelijken in de wetenschap?
Wat is observeren en vergelijken in de wetenschap?
Hoofdlijnen
- Welke organismen zijn meestal multicellulair met kerncellen zonder stijve celwand beweeglijk en heterotrofe die over het algemeen voedsel verteren in een interne kamer?
- Wat is FBS in laboratoriumtesten?
- Wat is de semantische organisatie van de menselijke taal?
- Wat is het verschil tussen isolatie van DNA of RNA met extractie?
- Hoe verschillen splitsing en embryo in betekenis?
- Waar heeft mucinase het grootste effect op?
- Welke van deze is een object dat draait om een lichaam dat groter is dan zichzelf?
- Micropropagatie van elite -soortenplanten?
- Onderzoek laat zien hoe slijm microben temt
- Destabilisatieprocessen in schuim

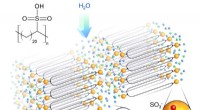
- Ingenieurs ontwerpen nieuwe vaste polymeerelektrolyt, weg vrijmaken voor veiliger, kleinere batterijen en brandstofcellen
- Wetenschappers vinden frustratie in batterijmaterialen

- Chemie gebruiken om het verschil tussen koude en warme koffie te ontdekken

- Persistente versus niet-persistente chemicaliën:levensduur, toxiciteit en impact op het milieu

 Borexino verzamelt de eerste directionele meting van sub-MeV zonne-neutrino's met behulp van een monolithische scintillatiedetector
Borexino verzamelt de eerste directionele meting van sub-MeV zonne-neutrino's met behulp van een monolithische scintillatiedetector  Wat als je nooit ouder bent geworden?
Wat als je nooit ouder bent geworden?  Wie was de eerste om die geocentrische theorie te bewijzen, toch?
Wie was de eerste om die geocentrische theorie te bewijzen, toch?  Eerste blik op waterstof op het grensvlak van metaal-op-metaalhydride
Eerste blik op waterstof op het grensvlak van metaal-op-metaalhydride Nieuwe methode zou kunnen onthullen welke genen van Neanderthalers zijn geërfd
Nieuwe methode zou kunnen onthullen welke genen van Neanderthalers zijn geërfd  De oppervlakken van Planet Mercury en je maan bevatten een aantal zeer grote kraters die waarschijnlijk het resultaat zijn van?
De oppervlakken van Planet Mercury en je maan bevatten een aantal zeer grote kraters die waarschijnlijk het resultaat zijn van?  Verborgen spin onthullen:nieuwe paden openen naar supergeleiders met hoge temperatuur
Verborgen spin onthullen:nieuwe paden openen naar supergeleiders met hoge temperatuur Wat zijn de eenheden voor stress?
Wat zijn de eenheden voor stress?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

