
Wetenschap
Vorming van natriumchloride:inzicht in ionische binding en keukenzout (NaCl)
1. Natrium (Na) heeft 1 valentie-elektron in de buitenste schil, waardoor het zeer reactief is. Het wil dit elektron kwijtraken om een stabiele elektronenconfiguratie te bereiken, zoals het dichtstbijzijnde edelgas (Neon).
2. Chloor (Cl) heeft 7 valentie-elektronen in zijn buitenste schil. Het heeft nog één elektron nodig om een stabiele elektronenconfiguratie te bereiken, zoals het dichtstbijzijnde edelgas (argon).
3. Elektronenoverdracht: Het natriumatoom staat zijn valentie-elektron gemakkelijk af aan het chlooratoom. Deze overdracht resulteert in een positief geladen natriumion (Na+) en een negatief geladen chloride-ion (Cl-).
4. Elektrostatische aantrekkingskracht: Vanwege hun tegengestelde ladingen worden het natriumion en het chloride-ion tot elkaar aangetrokken. Deze elektrostatische aantrekking vormt een ionische binding , waardoor ze bij elkaar worden gehouden als een molecuul natriumchloride (NaCl).
Belangrijkste inzichten:
* Ionische binding: Dit type binding treedt op wanneer een metaal (zoals natrium) een elektron verliest aan een niet-metaal (zoals chloor).
* Stabiele configuratie: Zowel natrium als chloor bereiken na de elektronenoverdracht een stabiele elektronenconfiguratie, waardoor de verbinding stabieler wordt dan de individuele atomen.
* Geen delen van elektronen: In tegenstelling tot covalente bindingen worden elektronen bij ionische bindingen volledig overgedragen en niet gedeeld.
Deze uitwisseling van elektronen is een fundamenteel proces in de chemie dat leidt tot de vorming van veel belangrijke verbindingen.
Hoofdlijnen
- Hoe verhoudt een wetenschappelijke theorie zich tot hypothese?
- Wat is het meest primitieve type bacteriën?
- Red Delicious of Wolf-appel? Braziliaanse savannevruchten met een hoog gehalte aan antioxidanten
- Waarom leven bacteriën?
- Wat is bemesting en schrijft zijn proces?
- Welk macromolecuul is verantwoordelijk voor het richten van de groei van het levende organisme?
- Wat is het celtype voor Kingdom Plantae?
- Heeft u twee ethische kwesties over biotechnologie?
- Welke ziekten hebben een kleine vitale capaciteit?
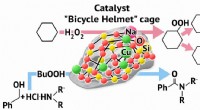
- Chemicus ontwikkelt nieuwe katalysator voor oxidatie en amidering
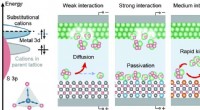
- Vulkaanvormige trend maakt rationeel ontwerp van polysulfidekatalysatoren in lithium-zwavelbatterijen mogelijk
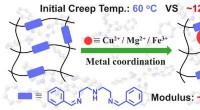
- Metaalcoördinatie maakt hoge temperatuur, kruipvast polyimine vitrimeer preparaat
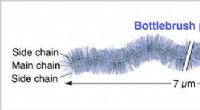
- 'S Werelds langste flessenborstelpolymeer ooit gesynthetiseerd
- Kristalheldere oplosmiddelfiltratie

 Hoe is waterstofbinding belangrijk voor het lichaam?
Hoe is waterstofbinding belangrijk voor het lichaam?  Wie ontdekken aluminium?
Wie ontdekken aluminium?  Hoe lang duurde het voordat Apollo ruimte kreeg en weer terug?
Hoe lang duurde het voordat Apollo ruimte kreeg en weer terug?  Wat voor soort energie is zon?
Wat voor soort energie is zon?  Hoe kunnen parasieten hun gastheren herkennen?
Hoe kunnen parasieten hun gastheren herkennen?  Welke chemische stof wordt gebruikt voor de detectie van sulfaat in waterige oplossing?
Welke chemische stof wordt gebruikt voor de detectie van sulfaat in waterige oplossing?  Waarom is orkaan Irma zo krachtig?
Waarom is orkaan Irma zo krachtig?  Welke drie functies moet een fossiel hebben om een indexfossiel te zijn?
Welke drie functies moet een fossiel hebben om een indexfossiel te zijn?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com


