
Wetenschap
De beweging van gasmoleculen begrijpen:willekeurige beweging en snelheid
1. Constante beweging: Gasmoleculen zijn altijd in beweging. Ze stoppen niet, zelfs niet bij extreem lage temperaturen. Deze constante beweging is te danken aan hun kinetische energie.
2. Willekeurige beweging: Gasmoleculen bewegen in onvoorspelbare richtingen. Hun paden veranderen voortdurend als gevolg van botsingen met elkaar en met de wanden van hun container.
3. Hoge snelheid: Gasmoleculen reizen met zeer hoge snelheden. De gemiddelde snelheid van een gasmolecuul hangt samen met de temperatuur:hoe hoger de temperatuur, hoe sneller de moleculen bewegen.
4. Botsingen: Gasmoleculen botsen voortdurend met elkaar en de wanden van hun container. Deze botsingen zijn elastisch, wat betekent dat kinetische energie behouden blijft.
5. Verspreiding: Gasmoleculen kunnen zich verspreiden en elke ruimte die ze innemen vullen door hun willekeurige beweging. Dit proces wordt diffusie genoemd.
6. Brownse beweging: Dit is de willekeurige beweging van deeltjes die in een vloeistof (zoals een gas of vloeistof) zijn gesuspendeerd als gevolg van botsingen met de omringende moleculen.
Belangrijkste concepten:
* Kinetische moleculaire theorie: Deze theorie verklaart het gedrag van gassen op basis van de beweging van hun moleculen.
* Temperatuur: Een maatstaf voor de gemiddelde kinetische energie van de moleculen in een stof.
* Druk: De kracht die gasmoleculen uitoefenen op de wanden van hun container.
Visualiseren van de beweging van gasmoleculen:
Stel je een zwerm bijen voor die door een kamer zoemt. De bijen zijn voortdurend in beweging, veranderen van richting en botsen tegen elkaar. Dit is vergelijkbaar met hoe gasmoleculen zich gedragen.
Laat het me weten als je meer informatie wilt over een van deze concepten!
 Is het correct om te zeggen dat slechts één waarneembare verandering bij een chemische reactie gaat?
Is het correct om te zeggen dat slechts één waarneembare verandering bij een chemische reactie gaat?  Onderzoekers onthullen spannende nieuwe manier om farmaceutische ingrediënten goedkoper en veiliger te produceren
Onderzoekers onthullen spannende nieuwe manier om farmaceutische ingrediënten goedkoper en veiliger te produceren Wat is de vergelijking voor N2O?
Wat is de vergelijking voor N2O?  Is deze koolstofketen verzadigd of onverzadigd C C?
Is deze koolstofketen verzadigd of onverzadigd C C?  Hoe kan de chemische activiteit van een element worden bepaald op basis van de locatie in de periodieke tabel?
Hoe kan de chemische activiteit van een element worden bepaald op basis van de locatie in de periodieke tabel?
 Studie suggereert dat de winters in La Niña kunnen blijven komen
Studie suggereert dat de winters in La Niña kunnen blijven komen Wat is een woord dat een gebied betekent omringd door water?
Wat is een woord dat een gebied betekent omringd door water?  Klimaatverandering - lessen van de Vikingen
Klimaatverandering - lessen van de Vikingen Waar komt het water dat we gebruiken om aan onze dagelijkse behoeften te voldoen?
Waar komt het water dat we gebruiken om aan onze dagelijkse behoeften te voldoen?  Alomtegenwoordig marien organisme dat samen met andere microben is geëvolueerd, bevordering van complexere ecosystemen
Alomtegenwoordig marien organisme dat samen met andere microben is geëvolueerd, bevordering van complexere ecosystemen
Hoofdlijnen
- Wat is de belangrijkste manier waarop cellen communiceren en activiteiten coördineren?
- Wat is een Erlenmeyer -kolf en zijn functie?
- Welk mechanisme is verantwoordelijk voor axonaal transport?
- Geen herten meer in de koplamp:onderzoek toont aan dat grote zoogdieren wel gebruik maken van wegkruisingsconstructies
- Hoe meer vergelijkbaar is, zijn de DNA -sequenties van twee soorten nauw verwant?
- Wat waren de redenen voor het opzetten van een menselijk genoomproject?
- Wat zijn de namen van 10 systemen in het menselijk lichaam?
- Wat is een kenmerk van de meeste dierencellen?
- De vitale rol van RNA in het leven:functies en belang
- Herontworpen plantenstof behandelt opioïde-verslaving bij muizen

- Zoete lysine-afbraak
- Microscopische strijdwagens leveren moleculen in onze cellen
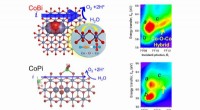
- Wetenschappers richten zich op röntgenstraling om nieuwe brandstofkatalysator te ontdekken
- Apparaat gebouwd voor extreme omgevingen kan de productie van Actinium-225 versnellen

 Zonneschermlagen volledig geïntegreerd op NASA's James Webb Space Telescope
Zonneschermlagen volledig geïntegreerd op NASA's James Webb Space Telescope Wat is de maat voor energiebewegingsdeeltjes?
Wat is de maat voor energiebewegingsdeeltjes?  CH3 en C2H5 begrijpen:methyl- en ethylgroepen uitgelegd
CH3 en C2H5 begrijpen:methyl- en ethylgroepen uitgelegd  Aanstaande Chinese lander zal insecten en planten naar het oppervlak van de maan brengen
Aanstaande Chinese lander zal insecten en planten naar het oppervlak van de maan brengen De kosten van eiwitpolymeergeneesmiddelen verlagen
De kosten van eiwitpolymeergeneesmiddelen verlagen NASA onthult compact centrum van tropische cycloon Vayus
NASA onthult compact centrum van tropische cycloon Vayus Welke planeet is 29 keer kleiner dan Jupiter?
Welke planeet is 29 keer kleiner dan Jupiter?  Zouten voor vakbondsadvocaten nemen stilletjes banen over in het NC Amazon-magazijn
Zouten voor vakbondsadvocaten nemen stilletjes banen over in het NC Amazon-magazijn
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

