
Wetenschap
Polaire moleculen begrijpen:typen, eigenschappen en voorbeelden
1. Water (H₂O): Water is het klassieke voorbeeld van een polair molecuul. Het zuurstofatoom is elektronegatiever dan de waterstofatomen, wat betekent dat het sterker elektronen aantrekt. Hierdoor ontstaat een gedeeltelijke negatieve lading op de zuurstof en gedeeltelijke positieve ladingen op de waterstofatomen. Deze ongelijkmatige ladingsverdeling maakt het molecuul polair.
2. Ammoniak (NH₃): Net als water is stikstof in ammoniak elektronegatiever dan waterstof. Hierdoor ontstaat een gedeeltelijke negatieve lading op de stikstof en gedeeltelijke positieve ladingen op de waterstofatomen. De vorm van het ammoniakmolecuul, met zijn eenzame elektronenpaar, draagt ook bij aan zijn polaire karakter.
3. Waterstofchloride (HCl): In HCl is chloor veel elektronegatiever dan waterstof. Dit resulteert in een sterke gedeeltelijk negatieve lading op chloor en een sterke gedeeltelijk positieve lading op waterstof. Dit significante verschil in elektronegativiteit maakt HCl een zeer polair molecuul.
Belangrijke opmerking: Polariteit komt voort uit de ongelijke verdeling van elektronen binnen een molecuul, meestal als gevolg van verschillen in elektronegativiteit tussen atomen. De vorm van het molecuul speelt ook een belangrijke rol.
 Robuust MOF-materiaal vertoont selectieve, volledig omkeerbare en herhaalbare opvang van giftig atmosferisch gas
Robuust MOF-materiaal vertoont selectieve, volledig omkeerbare en herhaalbare opvang van giftig atmosferisch gas Wat is leveroxidatietijd?
Wat is leveroxidatietijd?  pH van gedestilleerd water:neutraliteit en kleine variaties begrijpen
pH van gedestilleerd water:neutraliteit en kleine variaties begrijpen  Wat is de procentuele concentratie van een 0,1 N natriumhydoxide -oplossing?
Wat is de procentuele concentratie van een 0,1 N natriumhydoxide -oplossing?  Wat zijn 20 verschillende soorten antimicrobiële moleculen?
Wat zijn 20 verschillende soorten antimicrobiële moleculen?
 De geestelijke gezondheidstol van Puerto Ricos langdurige stroomuitval
De geestelijke gezondheidstol van Puerto Ricos langdurige stroomuitval Onderzoekers ontdekken dat pompen jong grondwater naar nieuwe diepten trekt, mogelijk met verontreinigingen op sleeptouw
Onderzoekers ontdekken dat pompen jong grondwater naar nieuwe diepten trekt, mogelijk met verontreinigingen op sleeptouw Wat is antropologie? Een blik op hoe mensen elkaar bestuderen
Wat is antropologie? Een blik op hoe mensen elkaar bestuderen  NASA-NOAA-satelliet helpt Teddy te bevestigen dat het nu een tropische storm is die record zet
NASA-NOAA-satelliet helpt Teddy te bevestigen dat het nu een tropische storm is die record zet Een invasief 'gigantisch' reptiel schuilt onder de veranda van Georgia, zeggen ambtenaren:dit is waarom het gevaarlijk is
Een invasief 'gigantisch' reptiel schuilt onder de veranda van Georgia, zeggen ambtenaren:dit is waarom het gevaarlijk is
Hoofdlijnen
- Zowel bacteriën als gist reproduceren zich volgens de aseksuele methode, maar hoe verschilt dit erin?
- Wat is een groep organen die samenwerken om nauw verwante functie uit te voeren?
- Hoe kan genetische variatie worden geïntroduceerd om organismen seksueel te reproduceren?
- Wat zijn defactoren die het proces van natuurlijke selectie beïnvloeden?
- Wat gebeurt er in meiose een die niet twee voorkomt?
- De combinatie van specifieke allelen waaruit een organisme bestaat, is organsim?
- Waarom geloven de meeste wetenschappers dat al het leven op aarde uit een enkele cel is geëvolueerd?
- Welke rol spelen eiwitten om de enorme hoeveelheid DNA een eukaryotische cel in kern te laten verlichten en hoe worden die genoemd?
- Ontwikkeling nabootsen in een petrischaaltje om te begrijpen hoe planten leven
- Spinazie gebruikt in neutronenstudies zou het geheim kunnen ontrafelen voor een sterkere plantengroei

- Stabilisatie van het borafluoreen-anion met carbenen
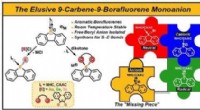
- Techniek kan goedkopere kunstmestproductie mogelijk maken

- Polyamiden van terpenen:Amorf Caramid-R en semi-kristallijn Caramid-S

- Onderzoekers ontdekken moleculaire mechanismen van oude kruidengeneesmiddelen
 Welke eenheden worden gebruikt om de hoeveelheid ruimte die door materie wordt ingenomen uit te drukken?
Welke eenheden worden gebruikt om de hoeveelheid ruimte die door materie wordt ingenomen uit te drukken?  Wat is de riem van vulkanische en seismische activiteit die grenst aan de meeste Pacific Rim?
Wat is de riem van vulkanische en seismische activiteit die grenst aan de meeste Pacific Rim?  Is het waar dat uw zonnestelsel één zon heeft?
Is het waar dat uw zonnestelsel één zon heeft?  Nu Shackletons Endurance is gevonden, wie bepaalt dan wat er met het beroemde scheepswrak gebeurt?
Nu Shackletons Endurance is gevonden, wie bepaalt dan wat er met het beroemde scheepswrak gebeurt? Een röntgentijdmachine?
Een röntgentijdmachine?  De chemische binding aangrenzende aminozuren wordt een genoemd?
De chemische binding aangrenzende aminozuren wordt een genoemd?  Welke plaatgrenzen ervaren de diepste aardbevingen en waarom?
Welke plaatgrenzen ervaren de diepste aardbevingen en waarom?  Met DISCO kunnen wetenschappers zeer reactief superoxide op koraalriffen meten
Met DISCO kunnen wetenschappers zeer reactief superoxide op koraalriffen meten
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

