
Wetenschap
Fluorgas vereist voor ethyleenconversie:een stapsgewijze berekening
1. Evenwichtige chemische vergelijking:
De reactie die je beschrijft is de fluorering van ethyleen (C₂H₄) om 1,2-difluorethaan (C₂H₄F₂) te produceren:
C₂H₄ + 2F₂ → C₂H₄F₂
2. Molberekeningen:
* Mollen C₂H₄F₂:
- Bereken de molaire massa van C₂H₄F₂:(2 * 12,01 g/mol) + (4 * 1,01 g/mol) + (2 * 19,00 g/mol) =66,06 g/mol
- Mol C₂H₄F₂ =(100 g) / (66,06 g/mol) =1,51 mol
* Mollen F₂:
- Uit de evenwichtsvergelijking blijkt dat voor elke mol C₂H₄F₂ 2 mol F₂ nodig is.
- Mol F₂ =(1,51 mol C₂H₄F₂) * (2 mol F₂ / 1 mol C₂H₄F₂) =3,02 mol F₂
3. Volumeberekening:
* Ideale gaswet:
- Ga uit van standaard temperatuur en druk (STP):0 °C (273,15 K) en 1 atm.
- Ideale gaswet:PV =nRT, waarbij:
- P =druk (atm)
- V =inhoud (L)
- n =moedervlekken
- R =ideale gasconstante (0,0821 L·atm/mol·K)
- T =temperatuur (K)
* Volume oplossen:
- V =(nRT) / P
- V =(3,02 mol * 0,0821 L·atm/mol·K * 273,15 K) / 1 atm
- V ≈ 67,5 L
Daarom is er ongeveer 67,5 liter fluorgas (F₂) nodig om 100 gram C₂H₄ om te zetten in C₂H₄F₂ bij STP.
Belangrijke opmerking: Fluorgas is uiterst reactief en gevaarlijk. Deze berekening is alleen bedoeld voor theoretisch begrip en mag niet in een laboratoriumomgeving worden uitgevoerd zonder de juiste veiligheidsmaatregelen en expertise.
 Trash tracking-satellieten helpen Indonesië om afval in zee aan te pakken
Trash tracking-satellieten helpen Indonesië om afval in zee aan te pakken Wat zijn vier niet-levende dingen in een woestijnecosysteem?
Wat zijn vier niet-levende dingen in een woestijnecosysteem?  Een slang of worm identificeren
Een slang of worm identificeren  De afname van de levensduur van bomen in bossen zou een deel van de stijging van de netto koolstofopname kunnen neutraliseren
De afname van de levensduur van bomen in bossen zou een deel van de stijging van de netto koolstofopname kunnen neutraliseren Door NASA geleide campagne bestudeert de iconische vulkanen van Hawaï
Door NASA geleide campagne bestudeert de iconische vulkanen van Hawaï
Hoofdlijnen
- Studie meldt eerste bewijs van sociale relaties tussen chimpansees en gorilla's
- Zou de enorme Pleistocene aap Gigantopithecus kunnen gedijen in de moderne wereld?
- Feiten over osmose voor kinderen
- Wat zijn de definities van theorie -evolutie?
- Organisme is voor de gemeenschap als orgaan voor?
- Hoe menselijke cellen en pathogene shigella de strijd aangaan
- Wat zijn de 3 systemen die ATP produceren?
- Wat zijn de klieren in wangen?
- Later, alligator? Een vijfde van alle reptielensoorten zou kunnen uitsterven, zegt een nieuwe studie
- Natuurkunde versus astma

- De degradatiestatus van moderne polymere museumartefacten kan worden geclassificeerd op basis van hun geur

- Ontwerpen van biologische beweging op nanometerschaal

- Wetenschappers vinden een goedkopere manier om OLED-schermen te verlichten

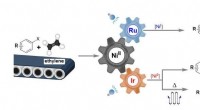
- Katalytische transformatie van ethyleen
 Hoe heet het als het licht door de lens van een telescoop reist?
Hoe heet het als het licht door de lens van een telescoop reist?  Wiskundige ontwikkelt model om verspreiding van in het water levende invasieve soorten te beheersen
Wiskundige ontwikkelt model om verspreiding van in het water levende invasieve soorten te beheersen Kan een verandering in materie plaatsvinden zonder dat energie wordt vrijgegeven of geabsorbeerd?
Kan een verandering in materie plaatsvinden zonder dat energie wordt vrijgegeven of geabsorbeerd?  Hoeveel centimeter is 11?
Hoeveel centimeter is 11?  Wat zijn twee lipidenfuncties?
Wat zijn twee lipidenfuncties?  Prokaryoten missen wat?
Prokaryoten missen wat?  Wat is de geschiedenis van bio -informatica?
Wat is de geschiedenis van bio -informatica?  Wanneer kondigde JFK aan dat we de maan gingen?
Wanneer kondigde JFK aan dat we de maan gingen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

